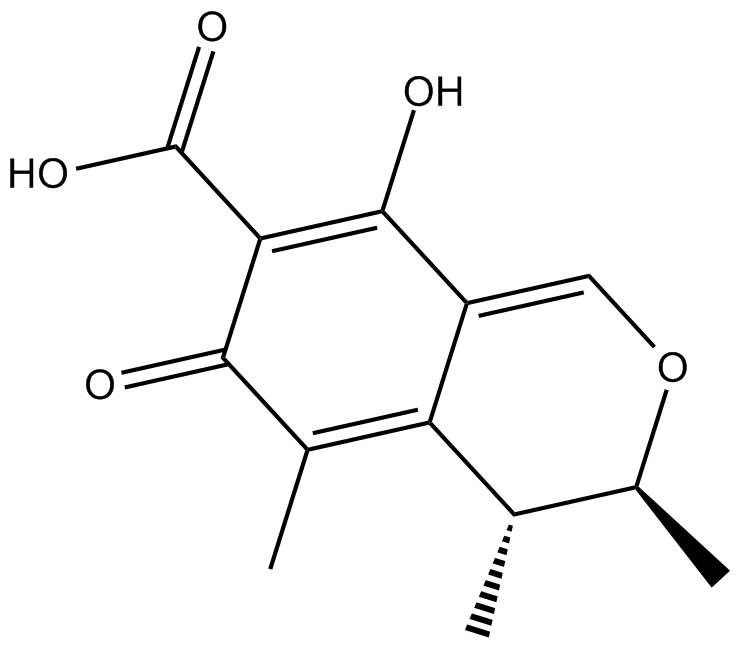
Apoptosis
As one of the cellular death mechanisms, apoptosis, also known as programmed cell death, can be defined as the process of a proper death of any cell under certain or necessary conditions. Apoptosis is controlled by the interactions between several molecules and responsible for the elimination of unwanted cells from the body.
Many biochemical events and a series of morphological changes occur at the early stage and increasingly continue till the end of apoptosis process. Morphological event cascade including cytoplasmic filament aggregation, nuclear condensation, cellular fragmentation, and plasma membrane blebbing finally results in the formation of apoptotic bodies. Several biochemical changes such as protein modifications/degradations, DNA and chromatin deteriorations, and synthesis of cell surface markers form morphological process during apoptosis.
Apoptosis can be stimulated by two different pathways: (1) intrinsic pathway (or mitochondria pathway) that mainly occurs via release of cytochrome c from the mitochondria and (2) extrinsic pathway when Fas death receptor is activated by a signal coming from the outside of the cell.
Different gene families such as caspases, inhibitor of apoptosis proteins, B cell lymphoma (Bcl)-2 family, tumor necrosis factor (TNF) receptor gene superfamily, or p53 gene are involved and/or collaborate in the process of apoptosis.
Caspase family comprises conserved cysteine aspartic-specific proteases, and members of caspase family are considerably crucial in the regulation of apoptosis. There are 14 different caspases in mammals, and they are basically classified as the initiators including caspase-2, -8, -9, and -10; and the effectors including caspase-3, -6, -7, and -14; and also the cytokine activators including caspase-1, -4, -5, -11, -12, and -13. In vertebrates, caspase-dependent apoptosis occurs through two main interconnected pathways which are intrinsic and extrinsic pathways. The intrinsic or mitochondrial apoptosis pathway can be activated through various cellular stresses that lead to cytochrome c release from the mitochondria and the formation of the apoptosome, comprised of APAF1, cytochrome c, ATP, and caspase-9, resulting in the activation of caspase-9. Active caspase-9 then initiates apoptosis by cleaving and thereby activating executioner caspases. The extrinsic apoptosis pathway is activated through the binding of a ligand to a death receptor, which in turn leads, with the help of the adapter proteins (FADD/TRADD), to recruitment, dimerization, and activation of caspase-8 (or 10). Active caspase-8 (or 10) then either initiates apoptosis directly by cleaving and thereby activating executioner caspase (-3, -6, -7), or activates the intrinsic apoptotic pathway through cleavage of BID to induce efficient cell death. In a heat shock-induced death, caspase-2 induces apoptosis via cleavage of Bid.
Bcl-2 family members are divided into three subfamilies including (i) pro-survival subfamily members (Bcl-2, Bcl-xl, Bcl-W, MCL1, and BFL1/A1), (ii) BH3-only subfamily members (Bad, Bim, Noxa, and Puma9), and (iii) pro-apoptotic mediator subfamily members (Bax and Bak). Following activation of the intrinsic pathway by cellular stress, pro‑apoptotic BCL‑2 homology 3 (BH3)‑only proteins inhibit the anti‑apoptotic proteins Bcl‑2, Bcl-xl, Bcl‑W and MCL1. The subsequent activation and oligomerization of the Bak and Bax result in mitochondrial outer membrane permeabilization (MOMP). This results in the release of cytochrome c and SMAC from the mitochondria. Cytochrome c forms a complex with caspase-9 and APAF1, which leads to the activation of caspase-9. Caspase-9 then activates caspase-3 and caspase-7, resulting in cell death. Inhibition of this process by anti‑apoptotic Bcl‑2 proteins occurs via sequestration of pro‑apoptotic proteins through binding to their BH3 motifs.
One of the most important ways of triggering apoptosis is mediated through death receptors (DRs), which are classified in TNF superfamily. There exist six DRs: DR1 (also called TNFR1); DR2 (also called Fas); DR3, to which VEGI binds; DR4 and DR5, to which TRAIL binds; and DR6, no ligand has yet been identified that binds to DR6. The induction of apoptosis by TNF ligands is initiated by binding to their specific DRs, such as TNFα/TNFR1, FasL /Fas (CD95, DR2), TRAIL (Apo2L)/DR4 (TRAIL-R1) or DR5 (TRAIL-R2). When TNF-α binds to TNFR1, it recruits a protein called TNFR-associated death domain (TRADD) through its death domain (DD). TRADD then recruits a protein called Fas-associated protein with death domain (FADD), which then sequentially activates caspase-8 and caspase-3, and thus apoptosis. Alternatively, TNF-α can activate mitochondria to sequentially release ROS, cytochrome c, and Bax, leading to activation of caspase-9 and caspase-3 and thus apoptosis. Some of the miRNAs can inhibit apoptosis by targeting the death-receptor pathway including miR-21, miR-24, and miR-200c.
p53 has the ability to activate intrinsic and extrinsic pathways of apoptosis by inducing transcription of several proteins like Puma, Bid, Bax, TRAIL-R2, and CD95.
Some inhibitors of apoptosis proteins (IAPs) can inhibit apoptosis indirectly (such as cIAP1/BIRC2, cIAP2/BIRC3) or inhibit caspase directly, such as XIAP/BIRC4 (inhibits caspase-3, -7, -9), and Bruce/BIRC6 (inhibits caspase-3, -6, -7, -8, -9).
Any alterations or abnormalities occurring in apoptotic processes contribute to development of human diseases and malignancies especially cancer.
References:
1.Yağmur Kiraz, Aysun Adan, Melis Kartal Yandim, et al. Major apoptotic mechanisms and genes involved in apoptosis[J]. Tumor Biology, 2016, 37(7):8471.
2.Aggarwal B B, Gupta S C, Kim J H. Historical perspectives on tumor necrosis factor and its superfamily: 25 years later, a golden journey.[J]. Blood, 2012, 119(3):651.
3.Ashkenazi A, Fairbrother W J, Leverson J D, et al. From basic apoptosis discoveries to advanced selective BCL-2 family inhibitors[J]. Nature Reviews Drug Discovery, 2017.
4.McIlwain D R, Berger T, Mak T W. Caspase functions in cell death and disease[J]. Cold Spring Harbor perspectives in biology, 2013, 5(4): a008656.
5.Ola M S, Nawaz M, Ahsan H. Role of Bcl-2 family proteins and caspases in the regulation of apoptosis[J]. Molecular and cellular biochemistry, 2011, 351(1-2): 41-58.
対象は Apoptosis
- Pyroptosis(15)
- Caspase(77)
- 14.3.3 Proteins(3)
- Apoptosis Inducers(71)
- Bax(15)
- Bcl-2 Family(136)
- Bcl-xL(13)
- c-RET(15)
- IAP(32)
- KEAP1-Nrf2(73)
- MDM2(21)
- p53(137)
- PC-PLC(6)
- PKD(8)
- RasGAP (Ras- P21)(2)
- Survivin(8)
- Thymidylate Synthase(12)
- TNF-α(141)
- Other Apoptosis(1145)
- Apoptosis Detection(0)
- Caspase Substrate(0)
- APC(6)
- PD-1/PD-L1 interaction(60)
- ASK1(4)
- PAR4(2)
- RIP kinase(47)
- FKBP(22)
製品は Apoptosis
- Cat.No. 商品名 インフォメーション
-
GC47042
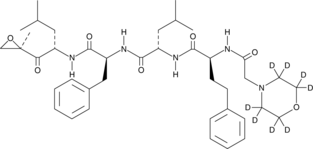
Carfilzomib-d8
カルフィルゾミブの定量化のための内部標準
-
GN10733
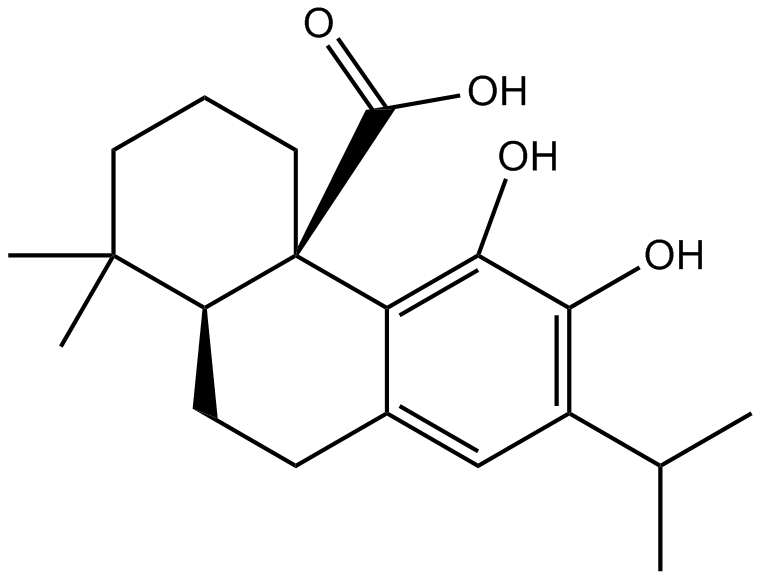
Carnosic acid
-
GC45679
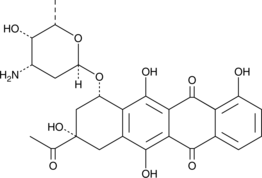
Carubicin
カルビシン (Carminomycin) は、微生物由来の化合物です。
-
GC64110
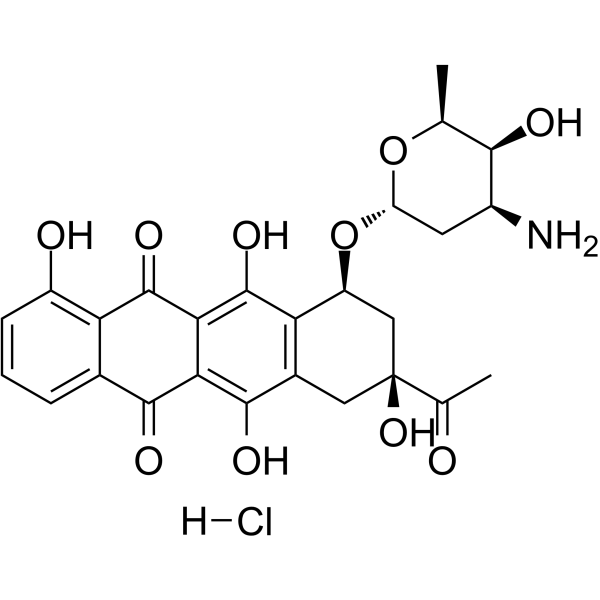
Carubicin hydrochloride
カルビシン塩酸塩は微生物由来の化合物です。
-
GC35612
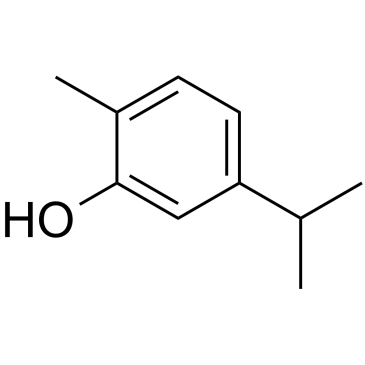
Carvacrol
カルバクロールは、Thymus mongolicus Ronn から分離されたモノテルペノイド フェノールです。
-
GC62442
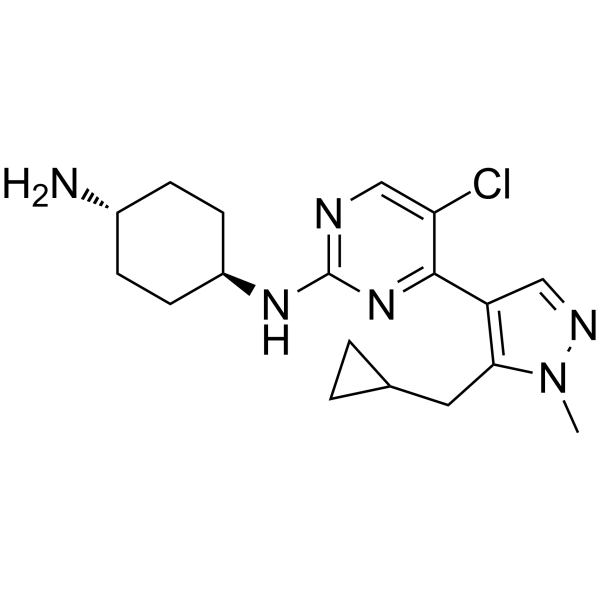
Casein Kinase inhibitor A51
カゼインキナーゼ阻害剤 A51 は、強力な経口活性カゼインキナーゼ 1α (CK1α) 阻害剤です。カゼインキナーゼ阻害剤 A51 は、白血病細胞のアポトーシスを誘導し、強力な抗白血病活性を持っています。
-
GC32841
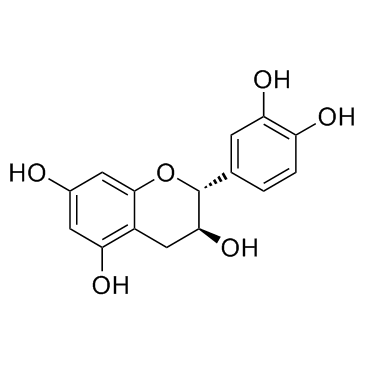
Catechin ((+)-Catechin)
カテキン ((+)-カテキン) ((+)-カテキン ((+)-カテキン)) は、1.4 μ の IC50 でシクロオキシゲナーゼ-1 (COX-1) を阻害します;M.
-
GN10543
caudatin
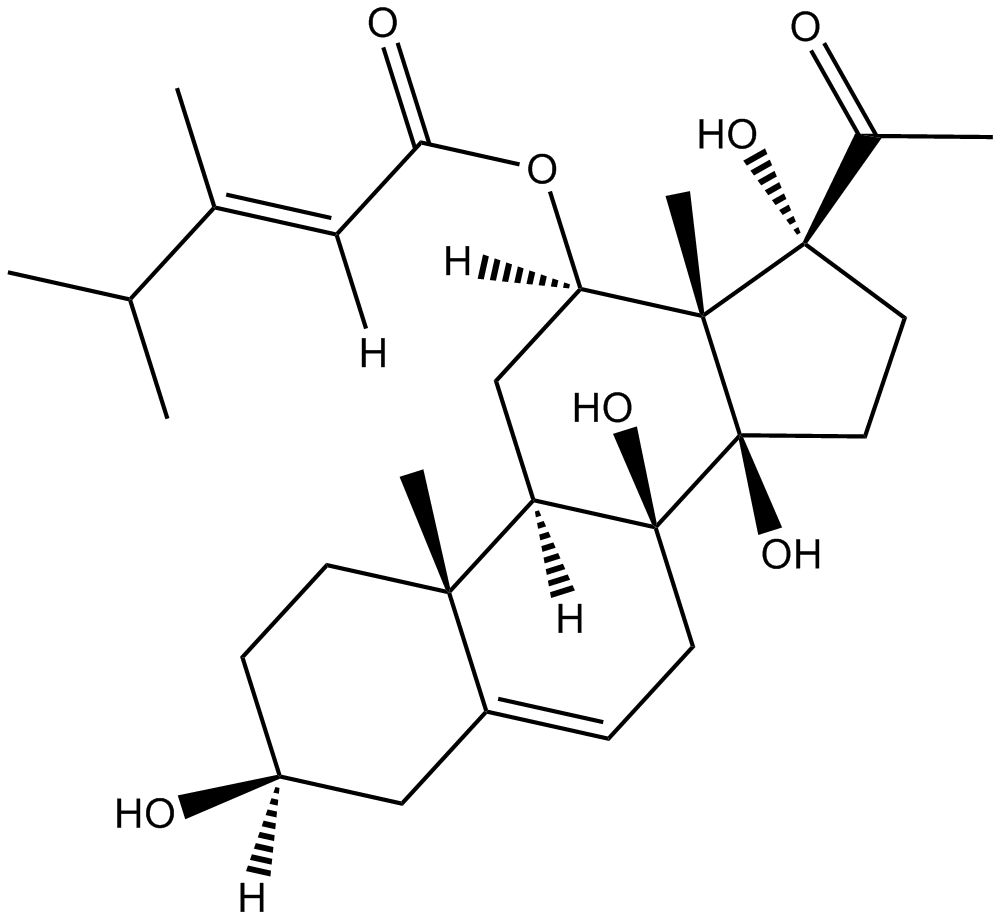
-
GC43149
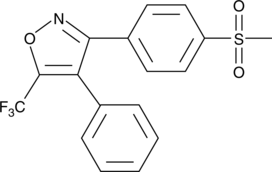
CAY10404
CAY10404 は、1 nM の IC50 と >500000 の選択指数 (SI; COX-1 IC50/COX-2 IC50) を持つ強力で選択的なシクロオキシゲナーゼ-2 (COX-2) 阻害剤です。
-
GC43150
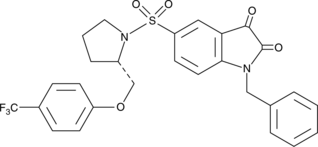
CAY10406
CAY10406は、カスパーゼ3および7を選択的に阻害するイサチンスルホンアミド化合物の三フルオロメチルアナログです。
-
GC43154
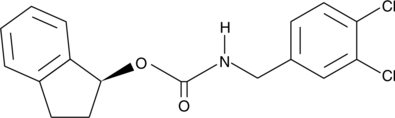
CAY10443
ミトコンドリアからのシトクロムcの放出は、カスパーゼ-9、Apaf-1、およびその他の成分を含む多量体複合体(時にはアポトソームと呼ばれる)の組み立てによってアポトーシスを誘発します。
-
GC43176
CAY10575
CAY10575 (化合物 8) は、IC50 が 0.075 μM の IKK2 阻害剤です。
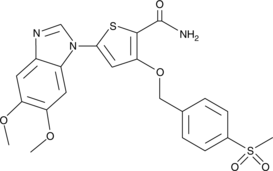
-
GC18530
CAY10616
レスベラトロールは、抗がん作用を持つ天然のポリフェノール抗酸化物質です。
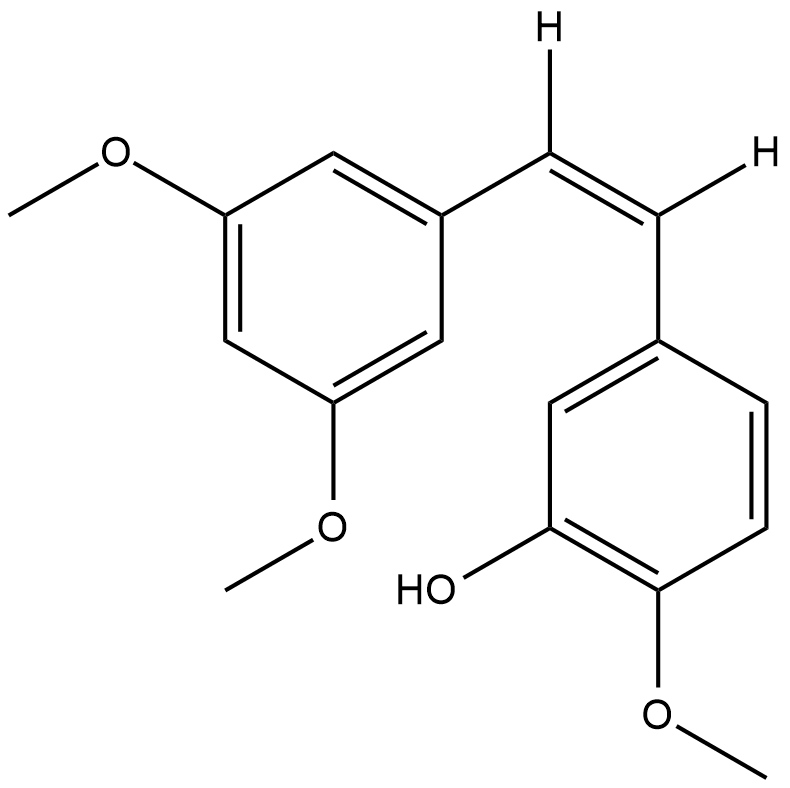
-
GC41317
CAY10625
サバイビンは、Smac/DIABLO、カスパーゼ-3、およびカスパーゼ-7を含むいくつかのタンパク質と相互作用してアポトーシス機能を阻害することにより細胞生存に関与する細胞内タンパク質です。
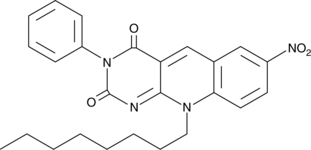
-
GC43189
CAY10681
腫瘍抑制因子p53の不活性化は、がんにおいてNF-κBを介したシグナル伝達の増加と一般的に重なります。
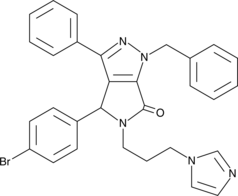
-
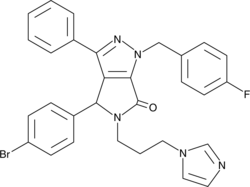
GC43190
CAY10682
(±)-Nutlin-3は、p53とその負の調節因子であるMdm2の相互作用をブロックします(IC50 = 90 nM)、p53によって調節された遺伝子の発現を誘導し、in vivoで腫瘍キシェンクラフトの成長を阻害します。
-
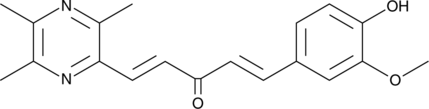
GC40650
CAY10706
CAY10706は、肺がん細胞に優先的に細胞内反応性酸素種の蓄積を促進するリグストラジン-クルクミンハイブリッドです。
-
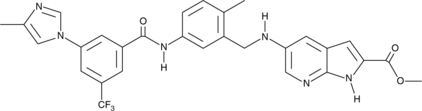
GC43198
CAY10717
CAY10717は、100 nMの濃度で酵素アッセイにおいて104つのキナーゼのうち34つを40%以上阻害する多目的キナーゼ阻害剤です。
-
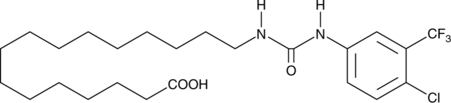
GC43203
CAY10726
CAY10726はアリールウレア脂肪酸です。
-
GC46113
CAY10744
トポイソメラーゼII-αの毒素
-
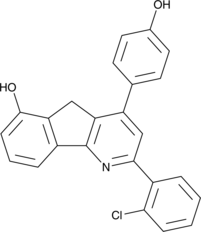
GC47053
CAY10746
ROCK1とROCK2の阻害剤
-
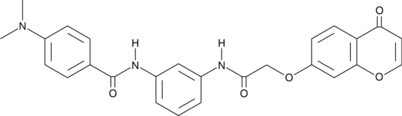
GC48392
CAY10747
Hsp90-Cdc37タンパク質間相互作用の阻害剤
-
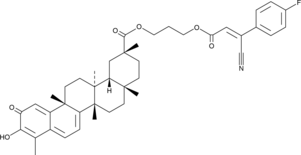
GC47055
CAY10749
Cay10749(化合物15)は、PARP-1、PARP-2、PI3K&&###945 ;, PI3K&&&&&&&&&&&&&&&&&&&777年にわたるPI3K/PI3KのPIC50値を持つ強力なPARP/PI3K阻害剤です。 offlineefficient_models_2022q2.md.en_ja_2022q2.mdCAY10749 is a highly effective anticancer compound targeted against a wide range of oncologic diseases.en_ja_2022q2.md
-
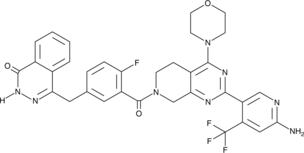
GC47057
CAY10755
抗がん活性を持つ真菌代謝物
-
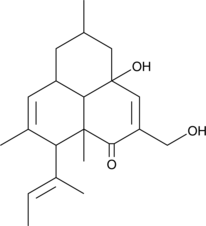
GC47061
CAY10763
IDO1とSTAT3活性化の二重阻害剤
-
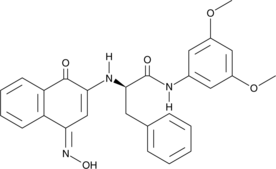
GC47065
CAY10773
ソラフェニブの誘導体
-
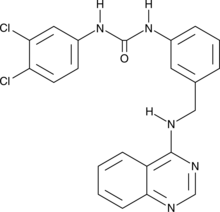
GC49080
CAY10786
CAY10786 (化合物 43) は、0.63 μ の IC50 を持つ GPR52 アンタゴニストです;M.
-
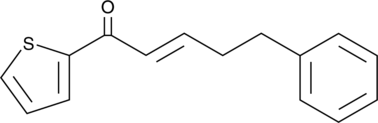
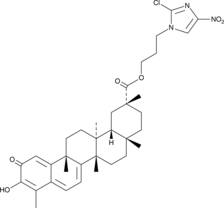
GC52245
CAY10792
抗がん剤
-
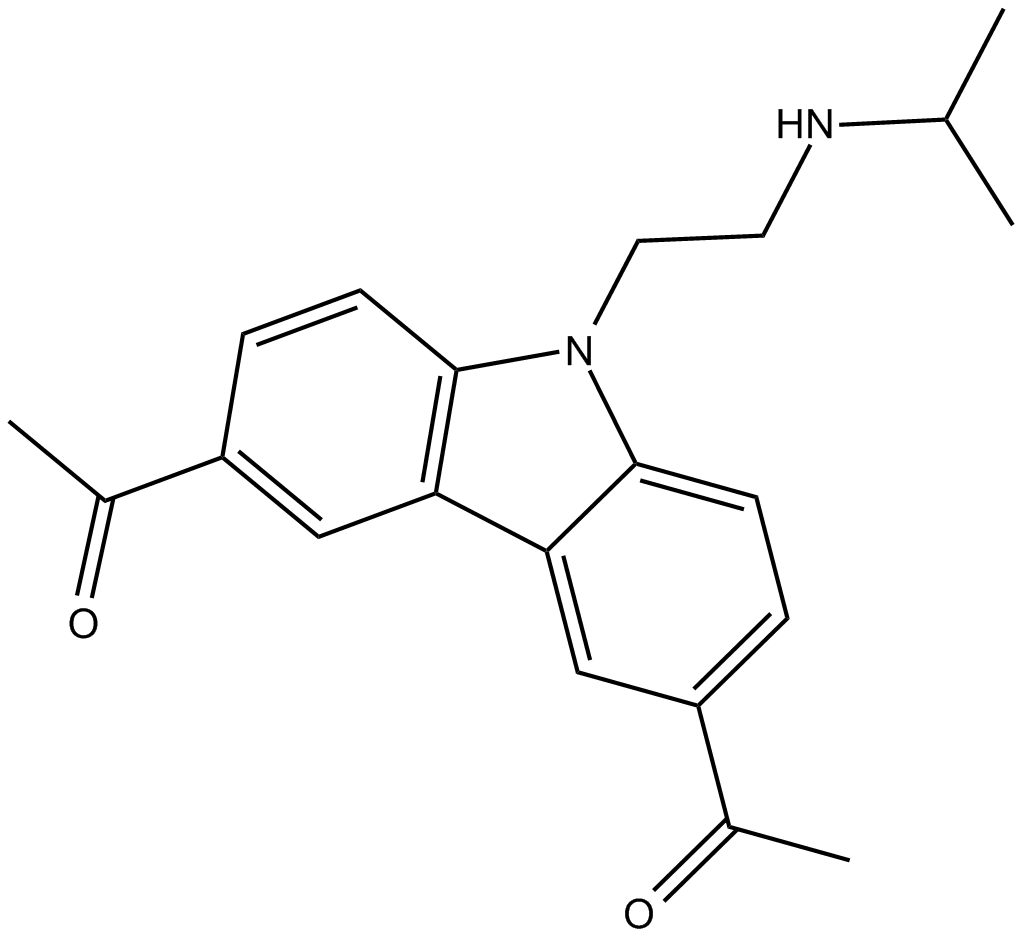
GC14634
CBL0137
p53を活性化し、NF-κBを抑制するクラキシン
-
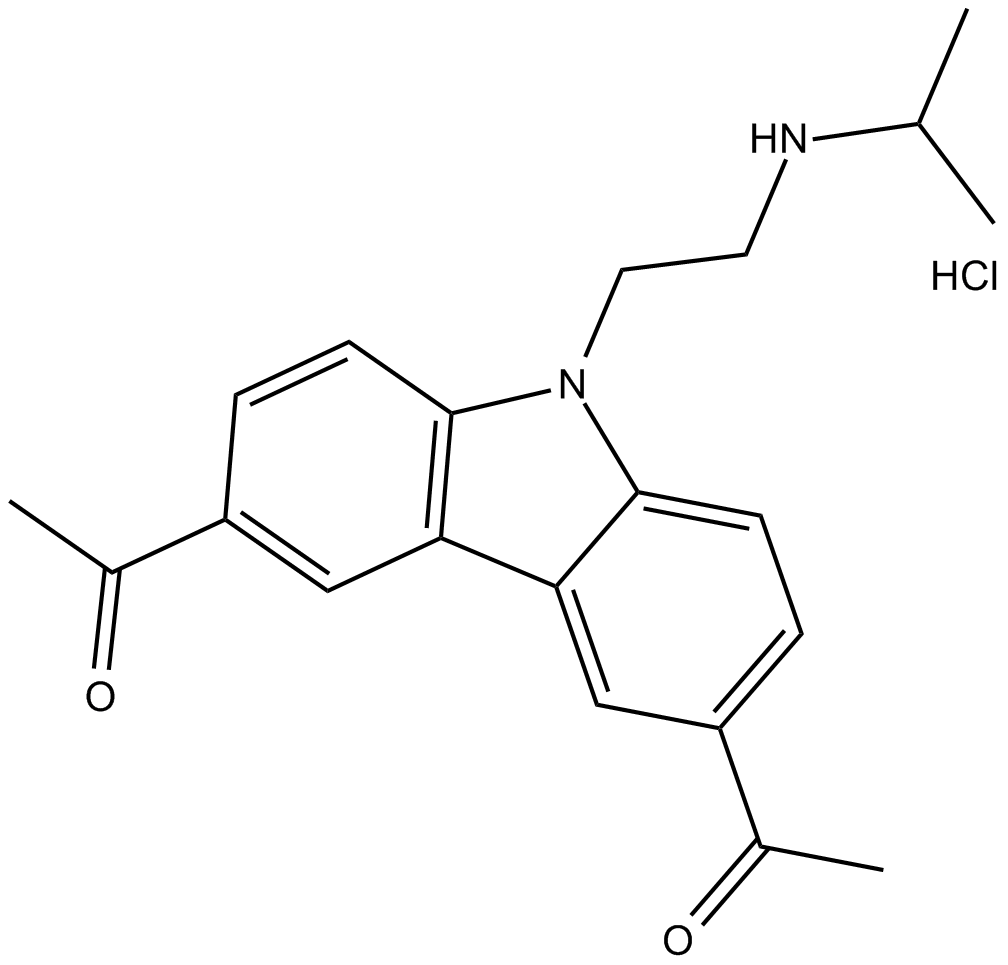
GC15394
CBL0137 (hydrochloride)
CBL0137 (塩酸塩) は、ヒストンシャペロンである FACT の阻害剤です。 CBL0137 (塩酸塩) は、p53 を活性化し、NF-κB をそれぞれ 0.37 および 0.47 μM の EC50 で阻害することもできます。
-
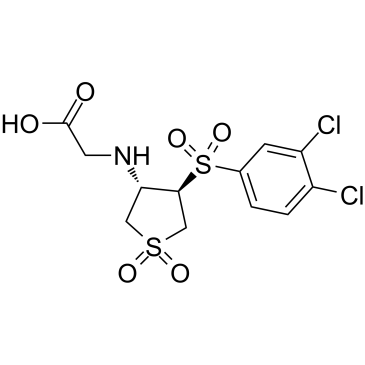
GC61636
CBR-470-2
グリシン置換類似体である CBR-470-2 は、NRF2 シグナル伝達を活性化できます。
-
GC13648
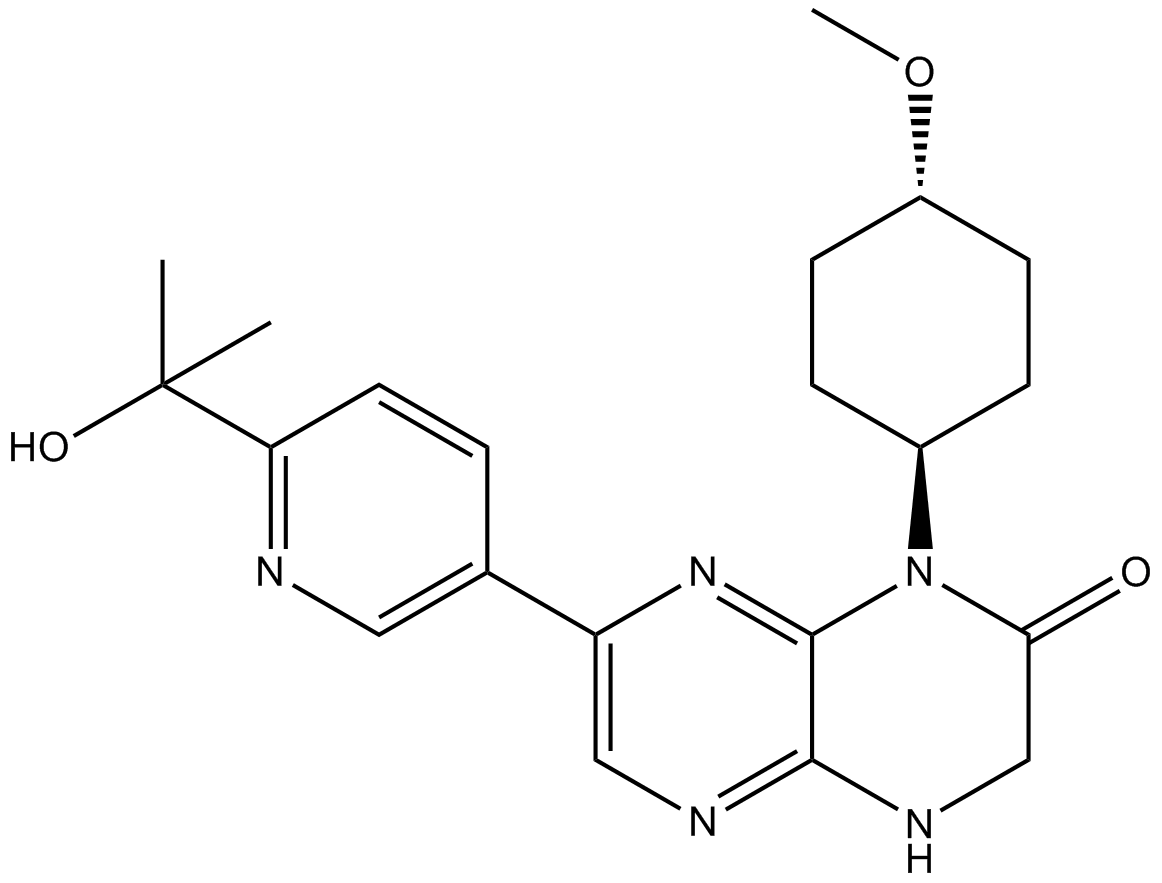
CC-223
CC-223 (CC-223) は、mTOR キナーゼの IC50 値が 16 nM である、mTOR キナーゼの強力で選択的な、経口で生物学的に利用可能な阻害剤です。 CC-223 は mTORC1 と mTORC2 の両方を阻害します。
-
GC39169
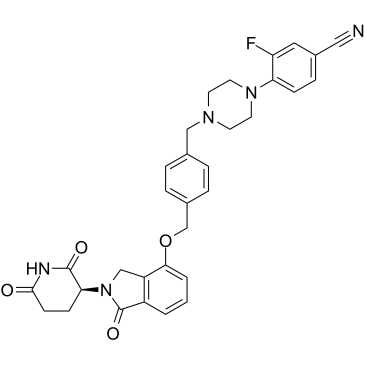
CC-92480
CC-92480 (CC-92480) は、セレブロン E3 ユビキチン リガーゼ調節薬 (CELMoD) であり、分子接着剤として機能します。 CC-92480 はセレブロンに高い親和性を示し、強力な抗骨髄腫活性をもたらします。
-
GC19088
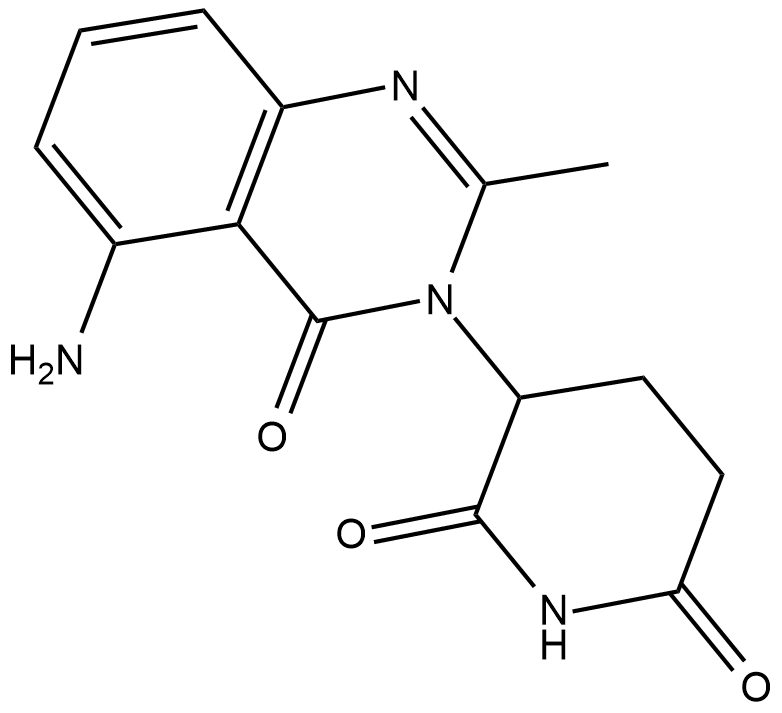
CC122
CC122 (CC 122) は、経口活性セレブロンモジュレーターです。
-
GC61532
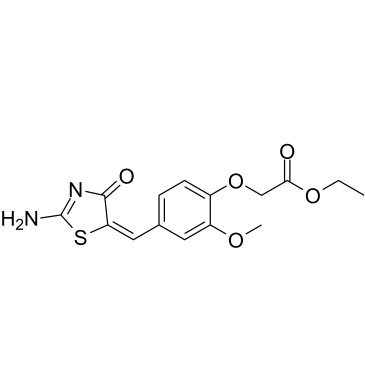
CCI-007
CCI-007 は、MLL 再構成を伴う乳児白血病に対する細胞傷害活性を持つ低分子であり、感受性細胞での IC50 値は 2.5 ~ 6.2 μM です。
-
GC12891
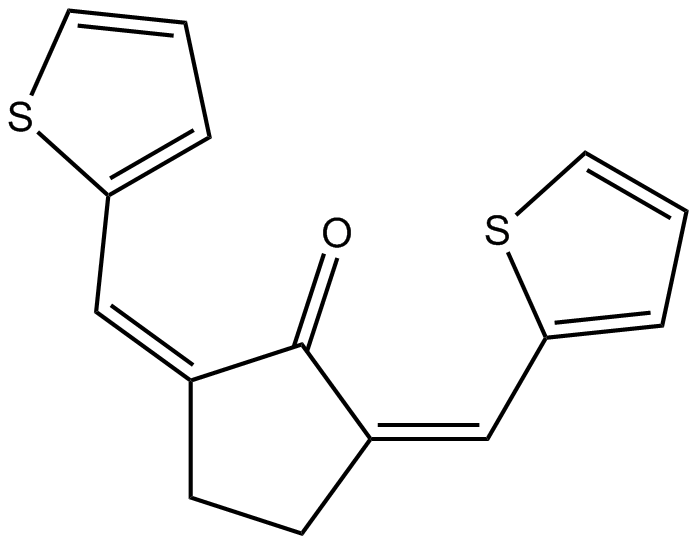
CCT007093
CCT007093 は効果的なプロテインホスファターゼ 1D (PPM1D Wip1) 阻害剤です。 Wip1 阻害は mTORC1 経路を活性化し、肝切除後の肝細胞増殖を促進します。
-
GC14566
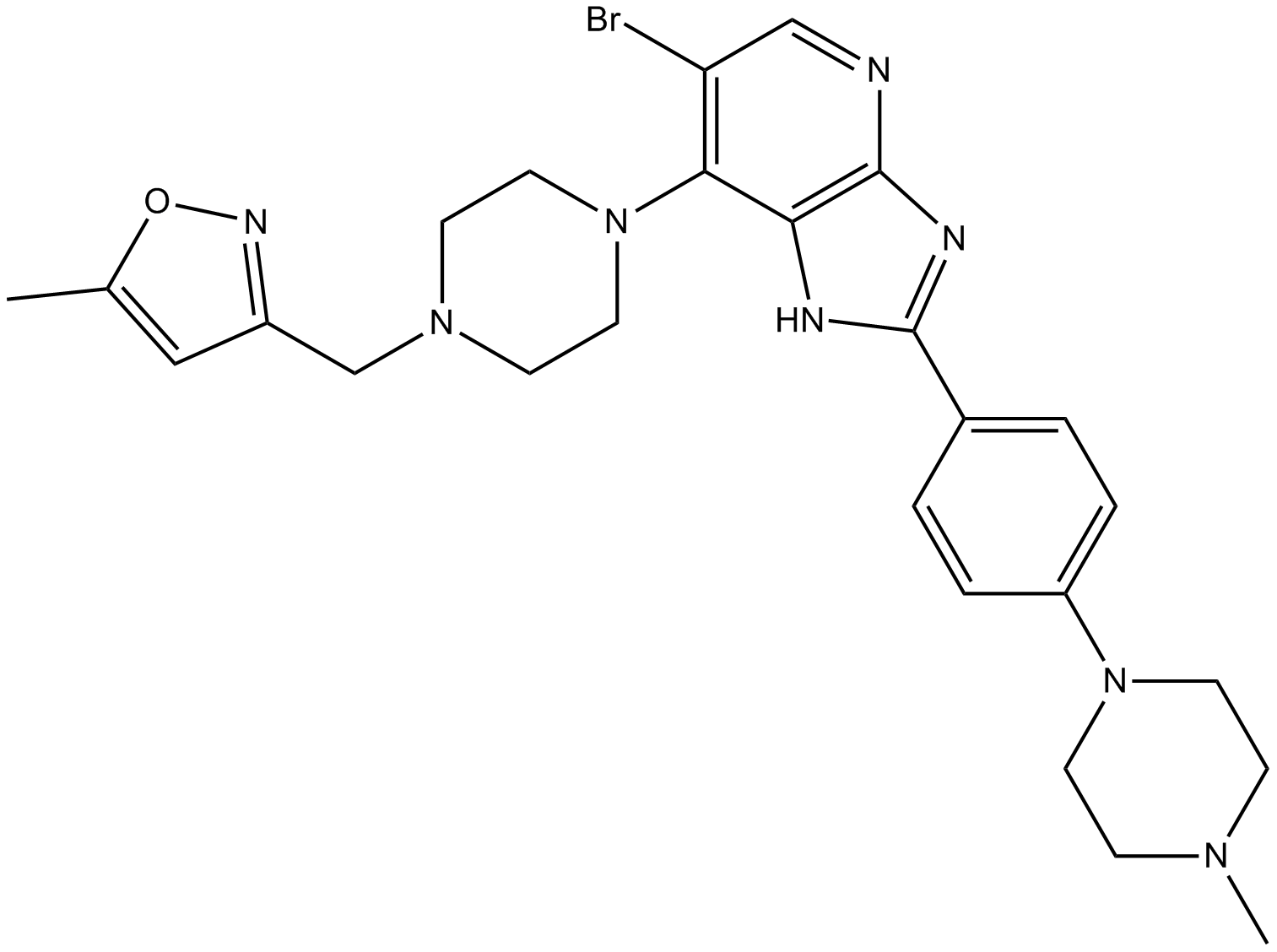
CCT137690
オーロラキナーゼとFLT3の阻害剤
-
GC62561
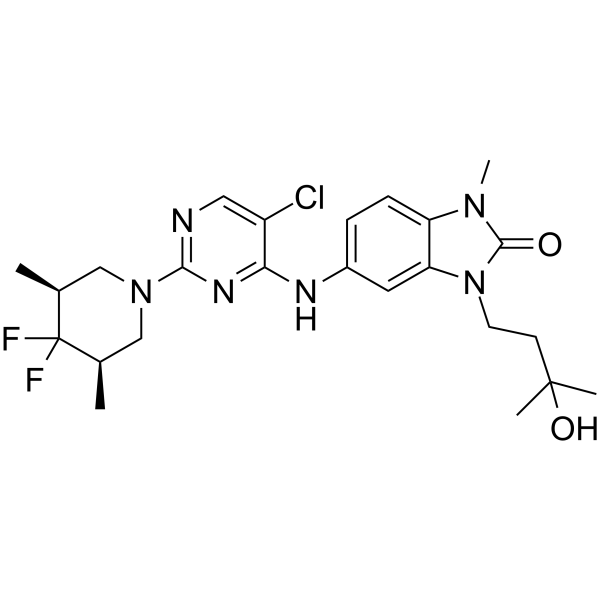
CCT369260
CCT369260 (化合物 1) は、抗腫瘍活性を有する経口活性 B 細胞リンパ腫 6 (BCL6) 阻害剤です。 CCT369260 (化合物 1) は 520 nM の IC50 を示します。
-
GC33337
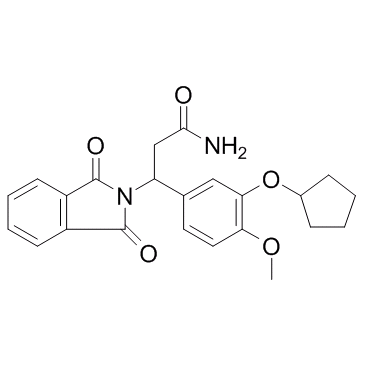
CDC801
CDC801 は強力な経口活性ホスホジエステラーゼ 4 (PDE4) であり、腫瘍壊死因子-α です。 (TNF-α) それぞれ 1.1 μM および 2.5 μM の IC50 を持つ阻害剤。
-
GC39555
CDDO-2P-Im
CDDO-2P-Im は、化学予防効果を持つ CDDO-イミダゾリドの類似体です。 CDDO-2P-Im は、マウス肺癌モデルの肺腫瘍のサイズと重症度を低下させることができます。
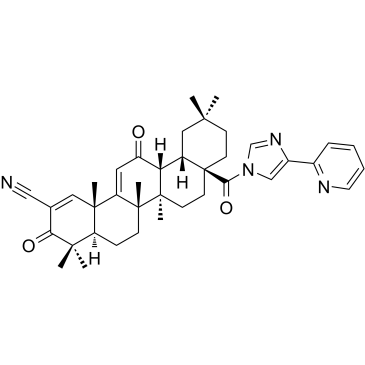
-
GC39556
CDDO-3P-Im
CDDO-3P-Im は、化学予防効果を持つ CDDO-イミダゾリドの類似体です。 CDDO-3P-Im は、マウス肺癌モデルの肺腫瘍のサイズと重症度を軽減することができます。 CDDO-3P-Im は、虚血/再灌流 (I/R) の研究に使用できる経口活性ネクロトーシス阻害剤です。
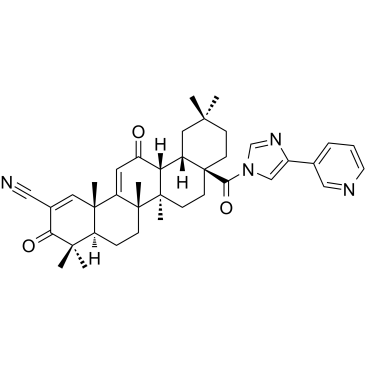
-
GC35629
CDDO-dhTFEA
CDDO-dhTFEA (RTA dh404) は合成オレアナン トリテルペノイド化合物で、Nrf2 を強力に活性化し、炎症誘発性転写因子 NF-κB を阻害します 。
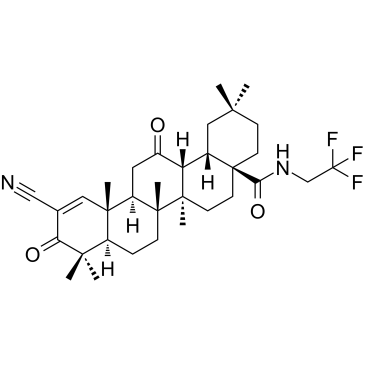
-
GC35630
CDDO-EA
CDDO-EA は、NF-E2 関連因子 2/抗酸化応答要素 (Nrf2/ARE) アクティベーターです。

-
GC32723
CDDO-Im (RTA-403)
CDDO-Im (RTA-403) (RTA-403) は Nrf2 および PPAR の活性化因子であり、PPARα の Kis は 232 および 344 nM です。およびPPARγ。
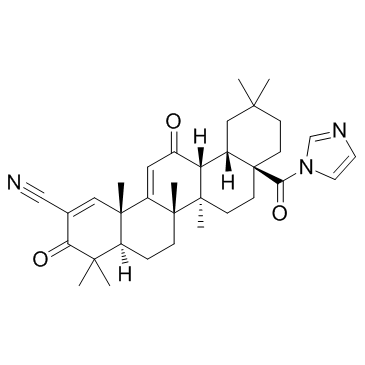
-
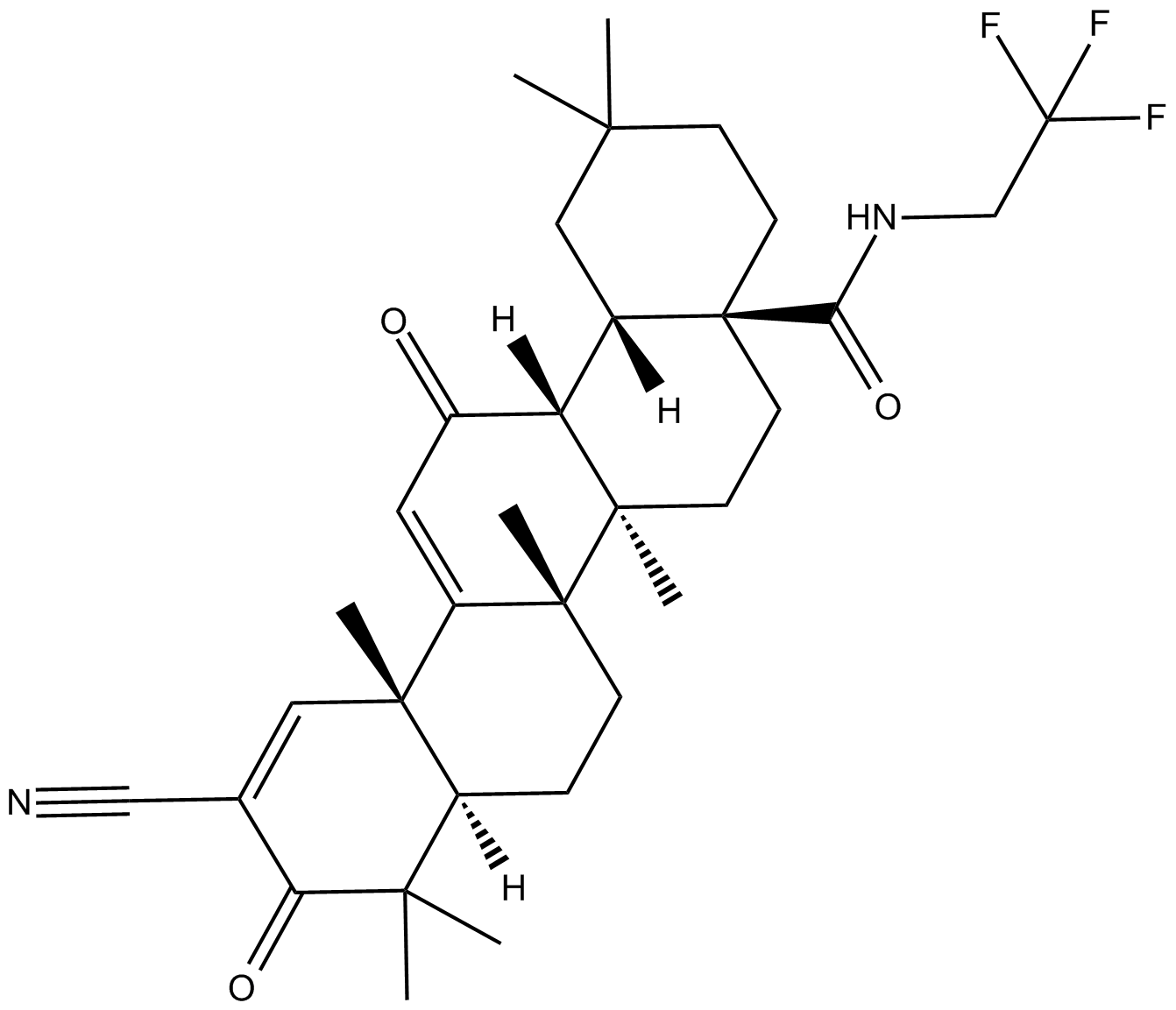
GC16625
CDDO-TFEA
Nrf2活性化剤
-
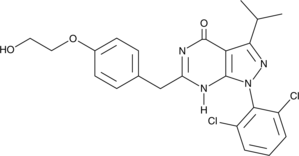
GC43217
CDK/CRK Inhibitor
CDK/CRK阻害剤は、体外でのIC50値が9〜839 nMのサイクリン依存性キナーゼ(CDK)およびCDK関連キナーゼ(CRK)の阻害剤です。
-
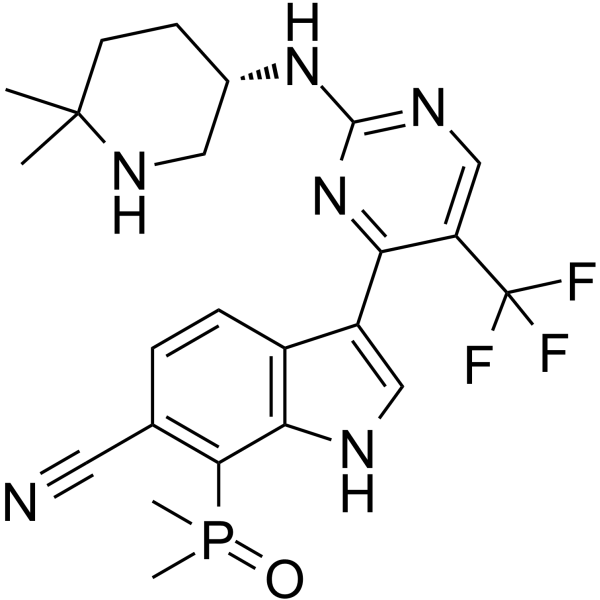
GC62596
CDK7-IN-3
CDK7-IN-3 (CDK7-IN-3) は、KD が 0.065 nM の経口活性で選択性の高い非共有結合の CDK7 阻害剤です。 CDK7-IN-3 は、CDK2 (Ki=2600 nM)、CDK9 (Ki=960 nM)、CDK12 (Ki=870 nM) に対して弱い阻害を示します。 CDK7-IN-3 は腫瘍細胞のアポトーシスを誘導し、抗腫瘍活性を持っています。
-
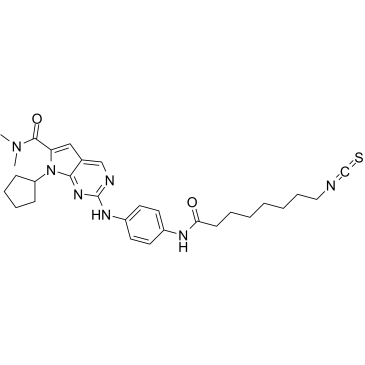
GC35636
CDK9-IN-7
CDK9-IN-7 (化合物 21e) は、選択的で非常に強力な経口活性 CDK9/サイクリン T 阻害剤 (IC50=11 nM) であり、他の CDK (CDK4/cyclinD=148 nM; CDK6/cyclinD= 145 nM)。 CDK9-IN-7 は明らかな毒性のない抗腫瘍活性を示します。 CDK9-IN-7 は、NSCLC 細胞のアポトーシスを誘導し、G2 期の細胞周期を停止させ、NSCLC の幹細胞性を抑制します。
-
GC19096
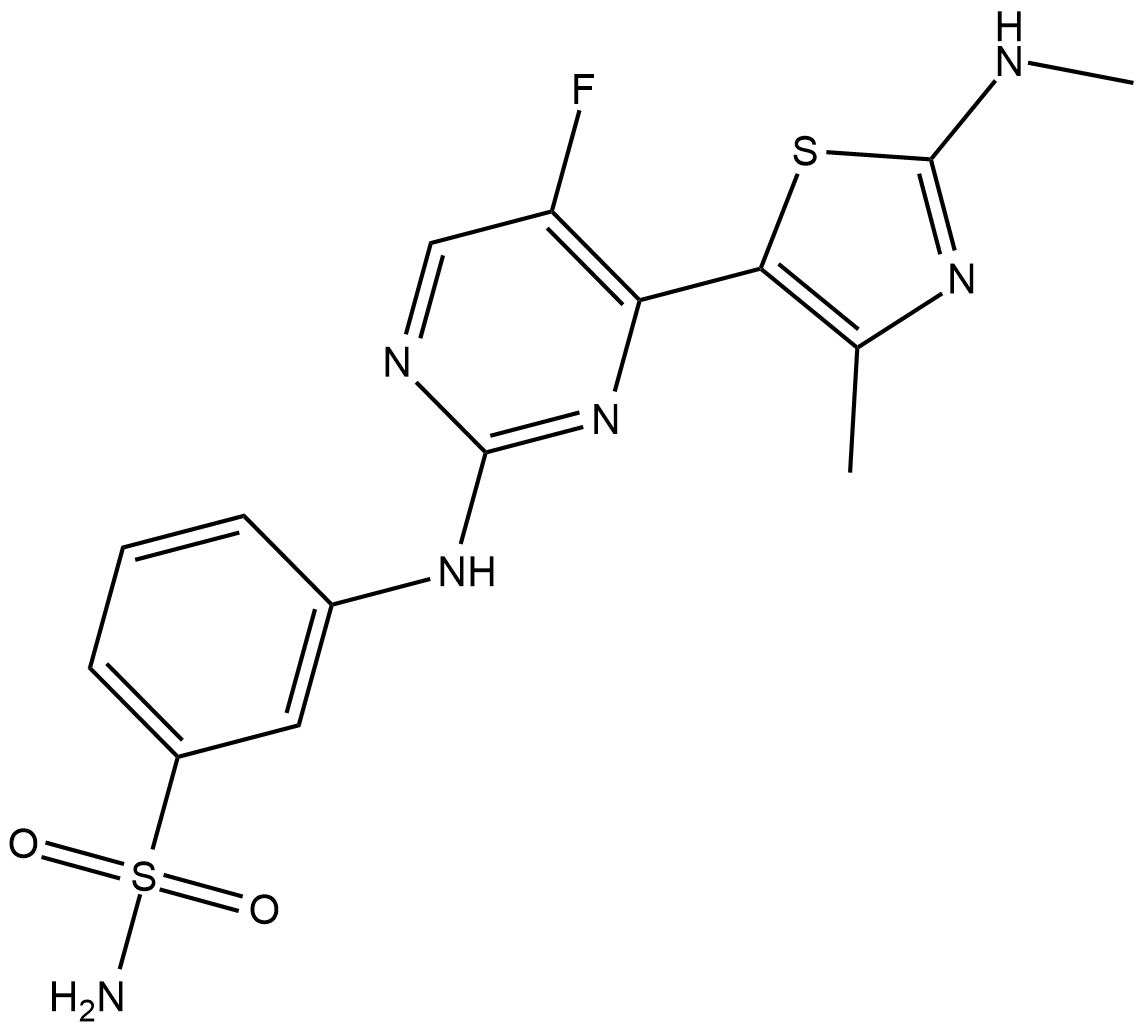
CDKI-73
CDKI-73 (LS-007) は、CDK9、CDK1、および CDK2 に対してそれぞれ 4 nM、4 nM、および 3 nM の Ki 値を持つ、経口活性で非常に有効な CDK9 阻害剤です。
-
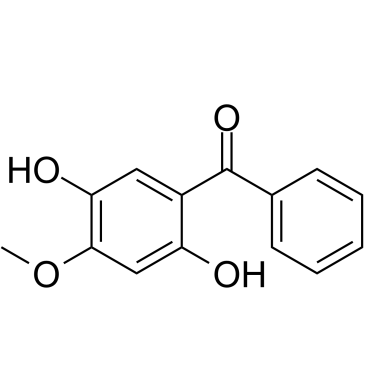
GC61865
Cearoin
Cearoin は、ROS の産生と ERK の活性化を通じて、オートファジーとアポトーシスを増加させます。
-
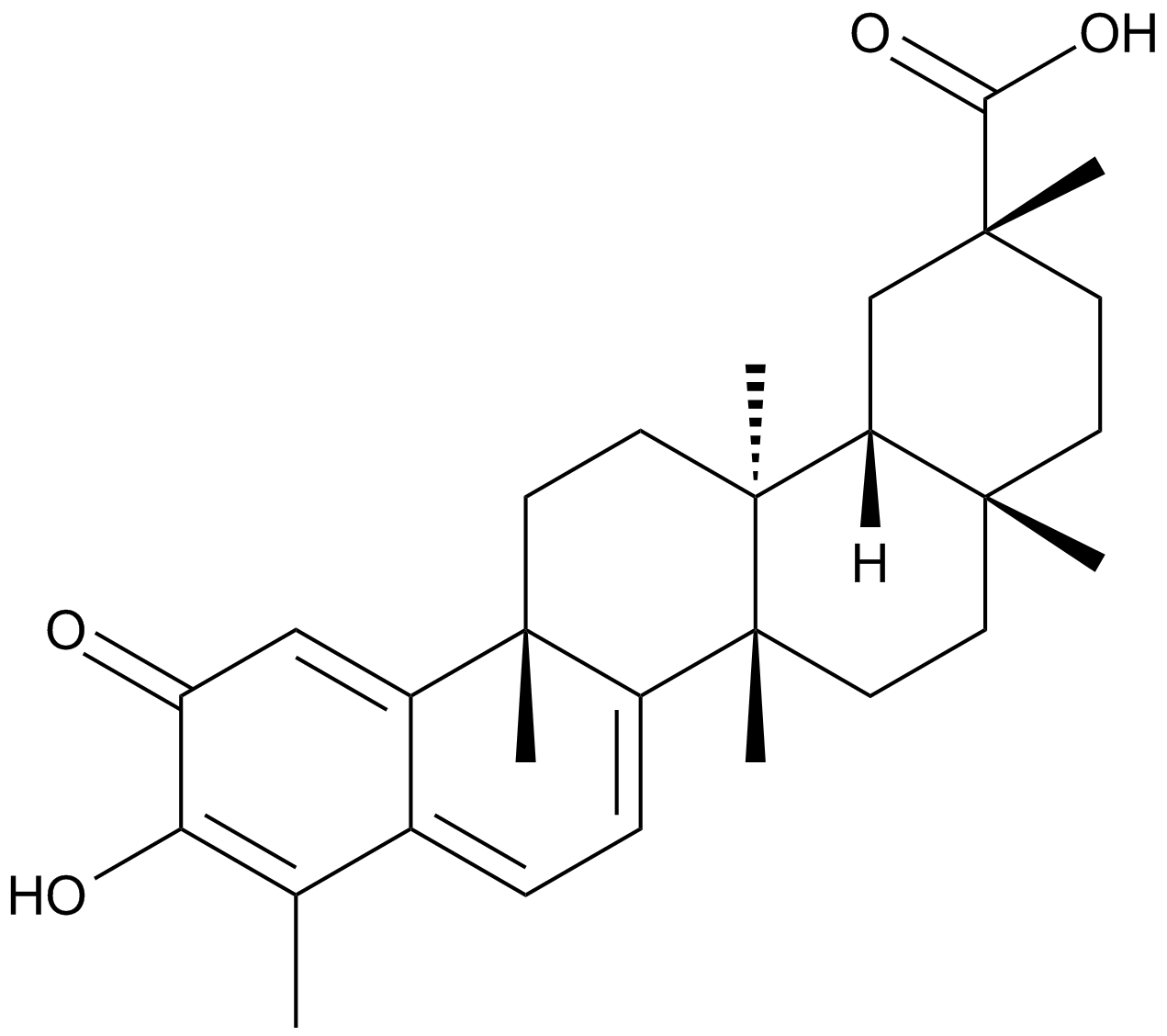
GC15083
Celastrol
トリテルペノイド抗酸化物質
-
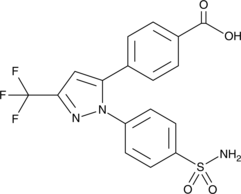
GC49152
Celecoxib Carboxylic Acid
セレコキシブの不活性代謝物
-
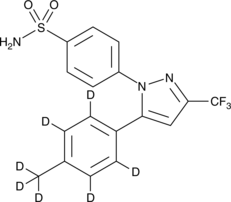
GC47070
Celecoxib-d7
セレコキシブの定量化のための内部標準
-
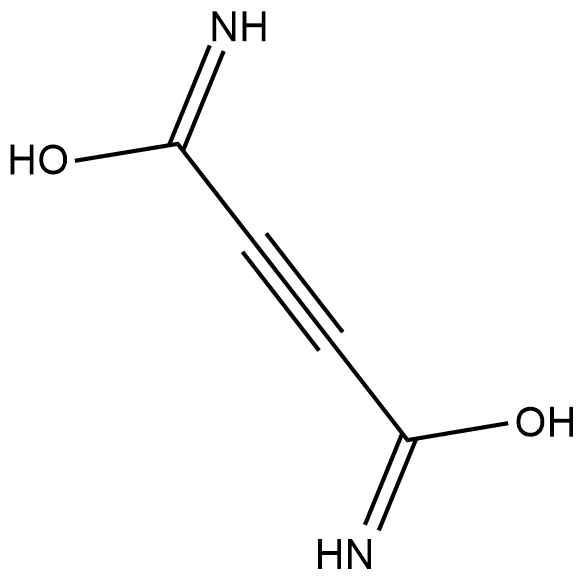
GC18392
Cellocidin
セロシジンは、元々Sから分離された抗生物質です。
-
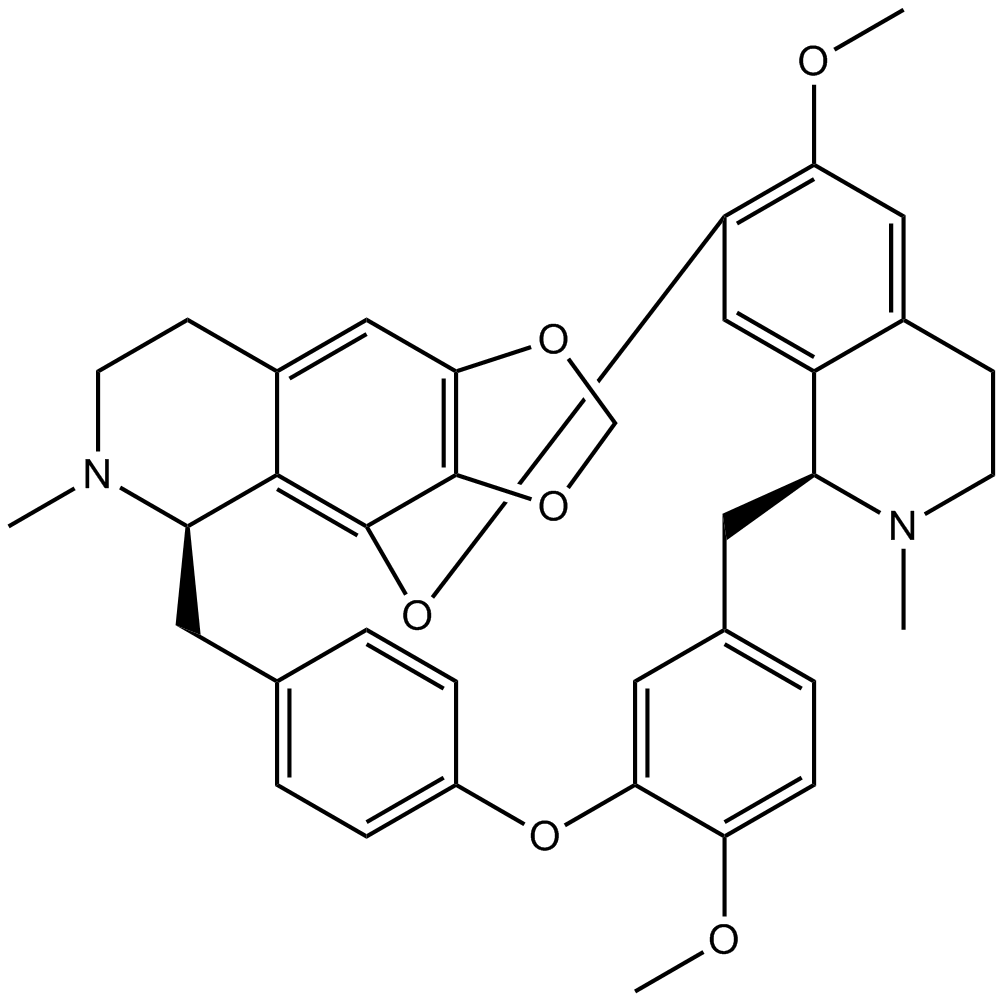
GN10113
Cepharanthine
-
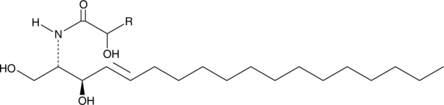
GC52489
Ceramide (hydroxy) (bovine spinal cord)
スフィンゴ脂質
-
GC52485
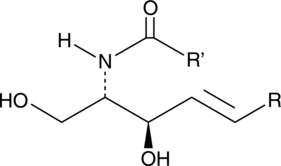
Ceramide (non-hydroxy) (bovine spinal cord)
スフィンゴ脂質
-
GC52486
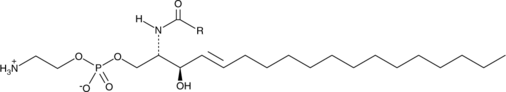
Ceramide Phosphoethanolamine (bovine)
スフィンゴ脂質
-
GC43229
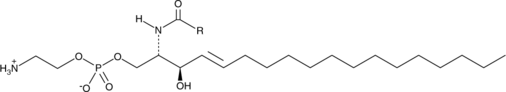
Ceramide Phosphoethanolamines (bovine)
セラミドホスホエタノールアミン(CPE)は、コリンではなくエタノールアミンを頭部基として含むスフィンゴ脂質の類似体です。
-
GC47073
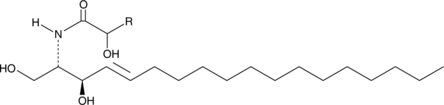
Ceramides (hydroxy)
ヒドロキシ脂肪酸を含むセラミドの混合物
-
GC43230
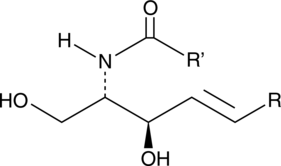
Ceramides (non-hydroxy)
セラミドは、スフィンゴミエリン酸化酵素の活性化によって生成されるか、またはセリンパルミトイルトランスフェラーゼとセラミド合成酵素の協調作用を必要とする新規合成経路を通じて生成されます。
-
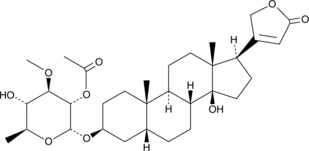
GC49706
Cerberin
細胞毒性と心臓調節作用を持つカルジャックスシド。
-
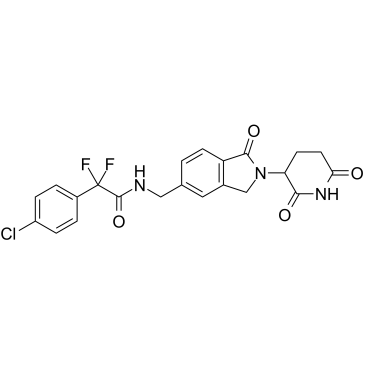
GC60688
Cereblon modulator 1
セレブロン モジュレーター 1 (CC-90009) は、クラス初の GSPT1 選択的セレブロン (CRBN) E3 リガーゼ モジュレーターであり、分子接着剤として機能します。
-
GC65487
Certolizumab pegol
セルトリズマブペゴル(セルトリズマブ)は、選択的にタンパク質分解酵素である腫瘍壊死因子-α(TNF-α)を標的とし中和する人工合成のポリエチレングリコール化されたヒューマナイズドモノクローナル抗体の抗原結合フラグメントです。

-
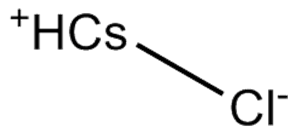
GC11543
Cesium chloride
-
GC11710
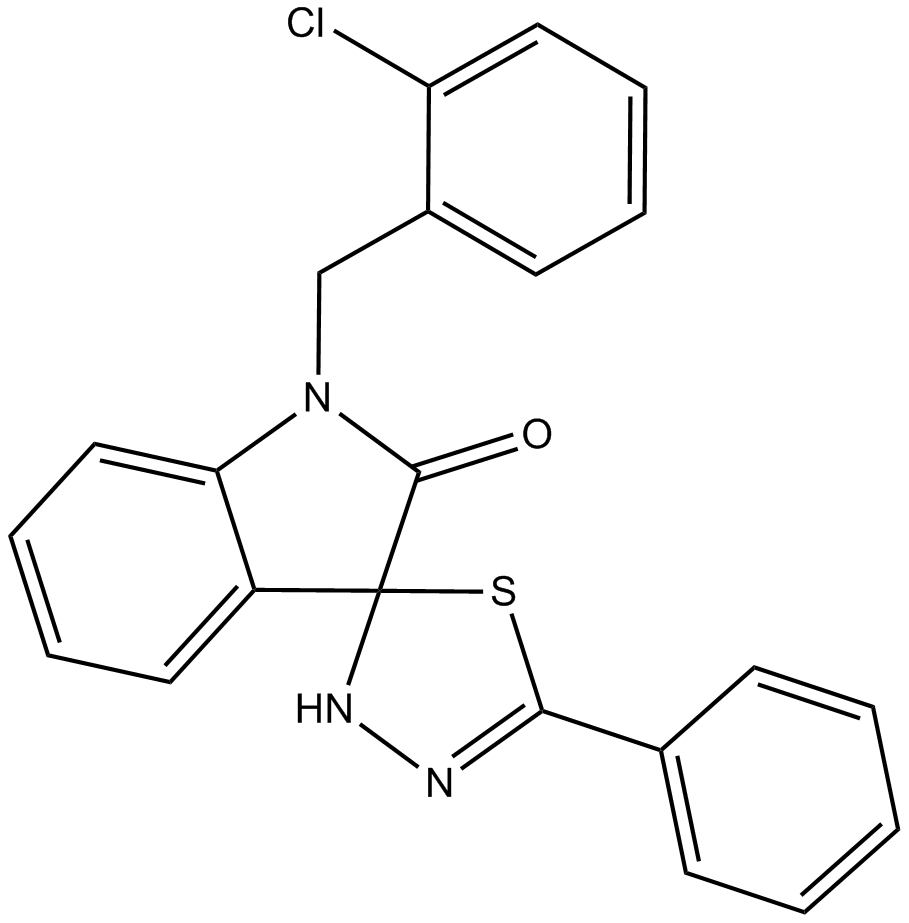
CFM 4
CFM 4 は、CARP-1/APC-2 結合の強力な低分子アンタゴニストです。 CFM 4 は、CARP-1 と APC-2 の結合を防ぎ、G2M 細胞周期停止を引き起こし、10-15 μM の IC50 範囲でアポトーシスを誘導します。 CFM 4 は、薬剤耐性のヒト乳癌細胞の増殖も抑制します。
-
GC35668
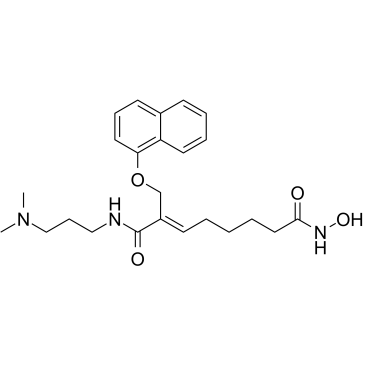
CG-200745
CG-200745 (CG-200745) は、触媒ポケットの底部で亜鉛に結合するヒドロキサム酸部分を有する、経口活性の強力な汎 HDAC 阻害剤です。 CG-200745 は、ヒストン H3 とチューブリンの脱アセチル化を阻害します。 CG-200745 は、p53 の蓄積を誘導し、p53 依存性のトランス活性化を促進し、MDM2 および p21 (Waf1/Cip1) タンパク質の発現を増強します。 CG-200745 は、ゲムシタビンおよび 5-フルオロウラシル (5-FU; ) に対するゲムシタビン耐性細胞の感受性を高めます。 CG-200745 はアポトーシスを誘導し、抗腫瘍効果があります。
-
GC10666
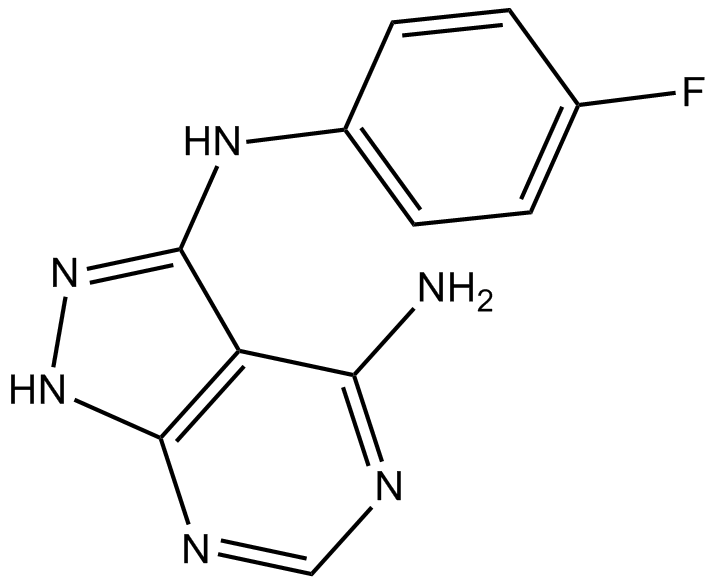
CGP 57380
CGP 57380 は、2.2 μM の IC50 で Mnk1 の選択的阻害剤として作用する細胞透過性ピラゾロ - ピリミジン化合物ですが、p38、JNK1、ERK1/2、PKC、または Src 様キナーゼに対する阻害活性はありません。
-
GC43234
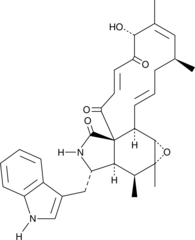
Chaetoglobosin A
ペニシリウム アクアマリニウムの抽出物に含まれる有効成分であるケトグロボシン A は、サイトカラサン ファミリーのメンバーです。
-
GC18536
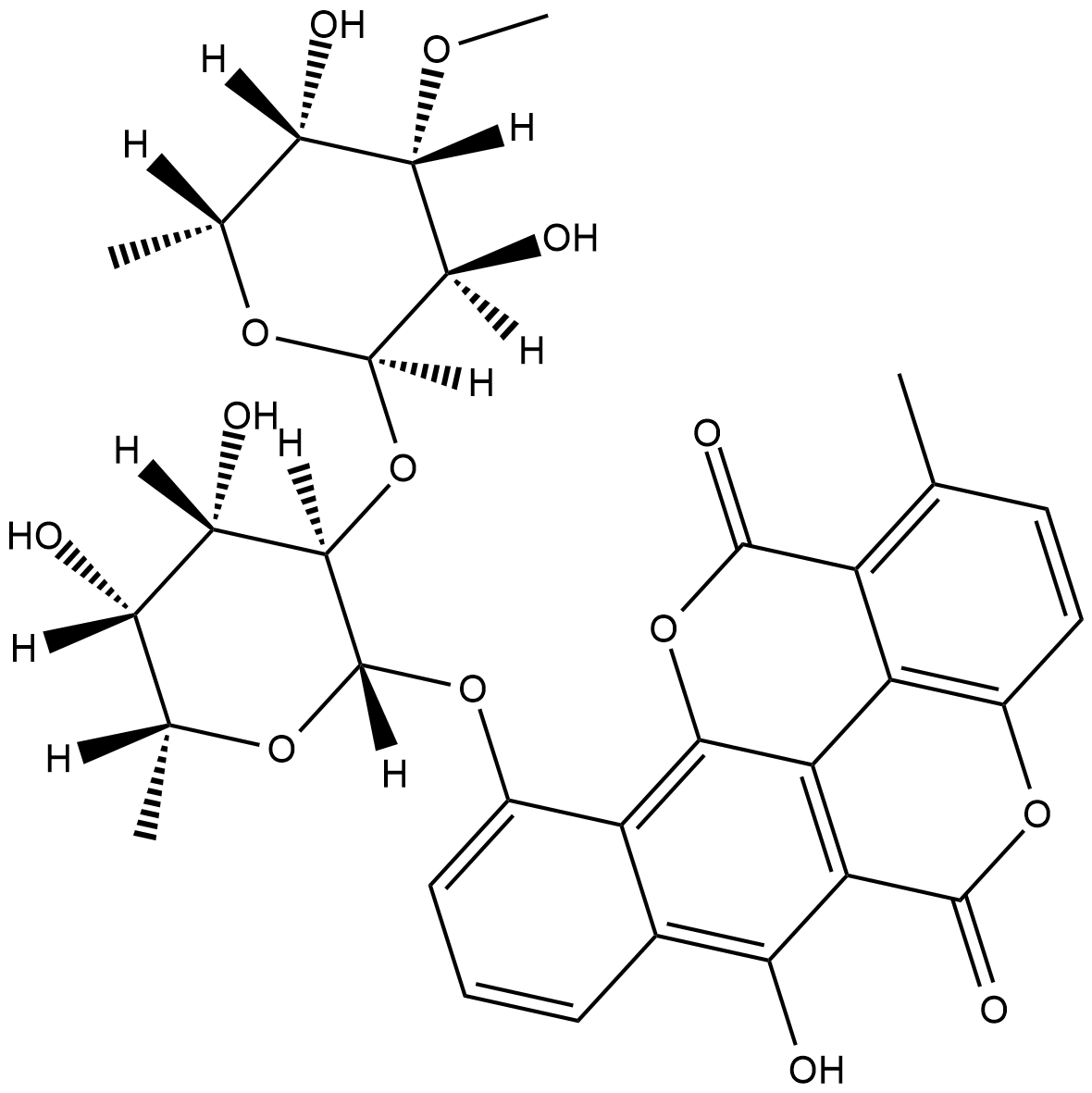
Chartreusin
シャルトリューシンは、元々Sから分離された抗生物質です。
-
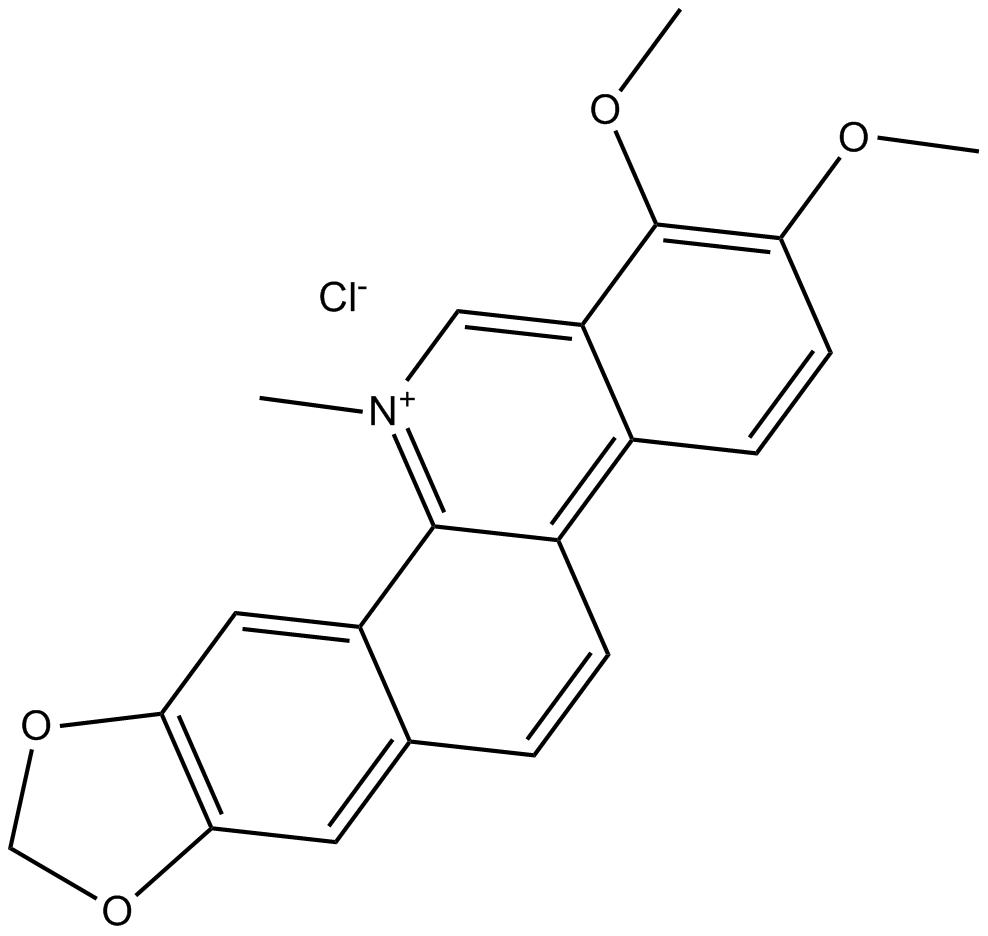
GN10463
Chelerythrine
-
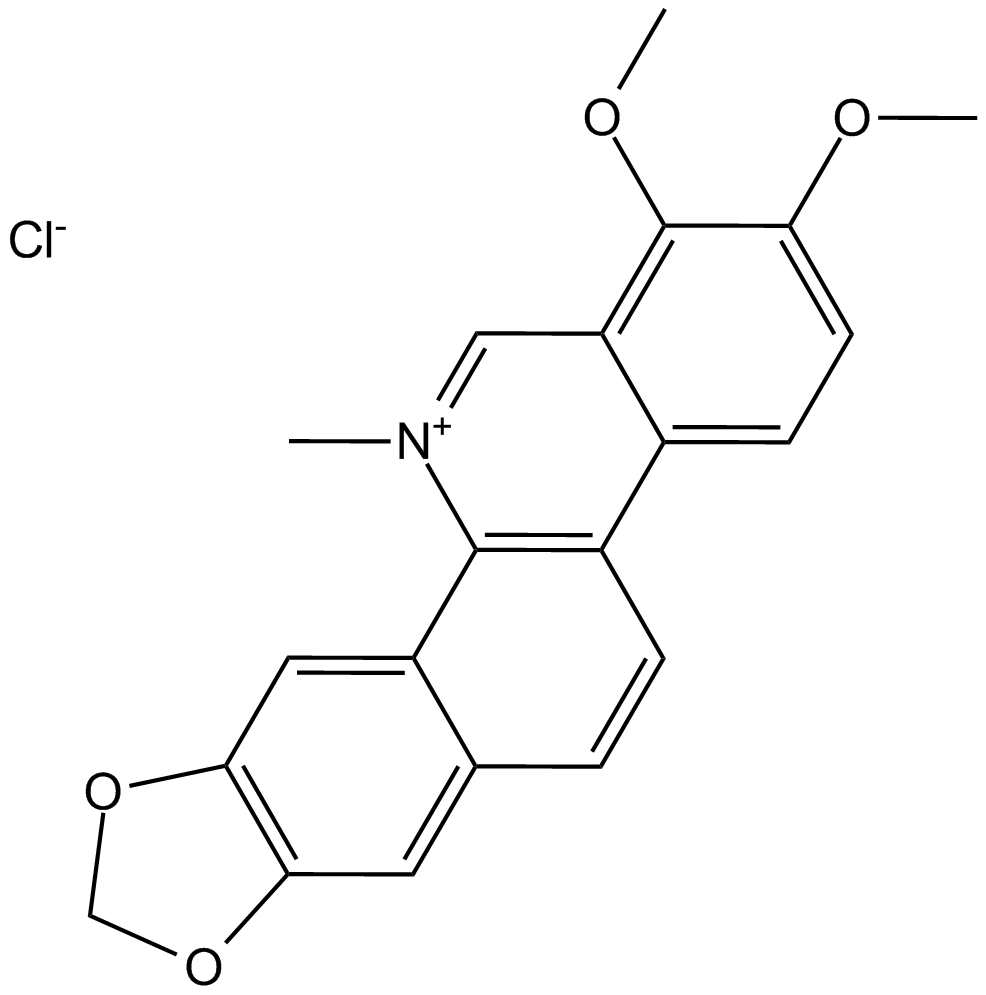
GC13065
Chelerythrine Chloride
PKCとBcl-xLの強力な阻害剤
-
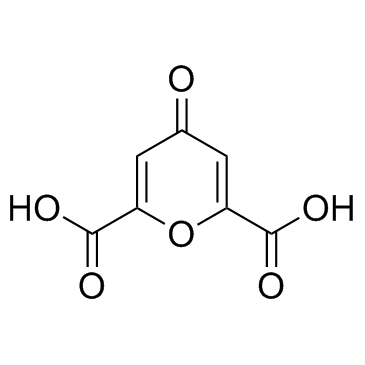
GC31886
Chelidonic acid
ケリドン酸はChelidonium majus Lの成分です。
-
GC40878
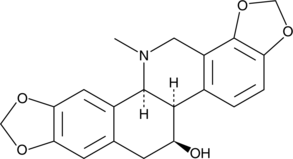
Chelidonine
ケリドニンはイソキノリン アルカロイドであり、Chelidonium majus L から分離できます。
-
GC43236
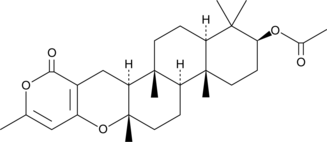
Chevalone B
シュヴァロンBは、元々キノコEから分離されたメロテルペノイドです。
-
GC43237
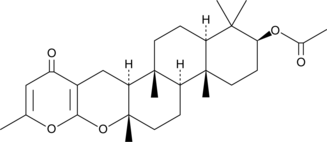
Chevalone C
メロテルペノイド真菌代謝産物であるシュバロン C は、25.00 μg/mL の IC50 値で抗マラリア活性を示します。
-
GC64993
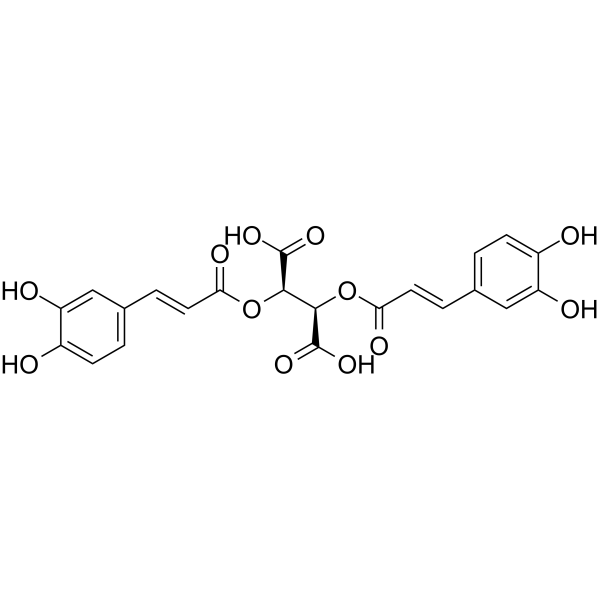
Chicoric acid
経口活性ジカフェイル酒石酸であるチコリ酸 (Cichoric acid) は、活性酸素種 (ROS) の生成を誘導します。
-
GC15739
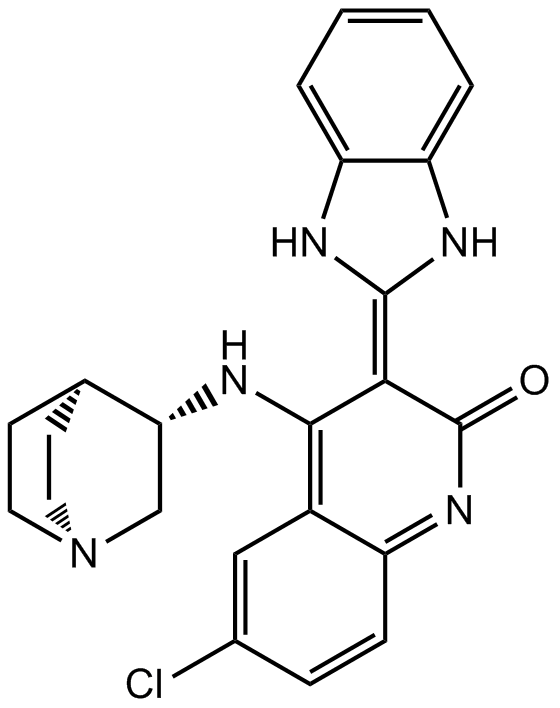
CHIR-124
CHIR-124 は、IC50 が 0.3 nM の強力で選択的な Chk1 阻害剤であり、PDGFR と FLT3 を強力に標的とし、IC50 は 6.6 nM と 5.8 nM です。
-
GC43239
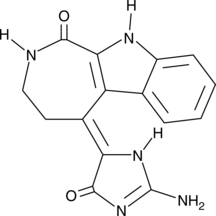
Chk2 Inhibitor
Chk2 阻害剤 (化合物 1) は、チェックポイントキナーゼ 2 (Chk2) の強力かつ選択的な阻害剤であり、Chk2 と Chk1 の IC50 はそれぞれ 13.5 nM と 220.4 nM です。 Chk2 阻害剤は、強力な毛細血管拡張性運動失調症変異 (ATM) 依存性 Chk2 を介した放射線防護効果を誘発することができます。
-
GC45717
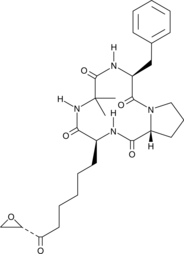
Chlamydocin
真菌の代謝産物であるクラミドシンは、IC50 が 1.3 nM の非常に強力な HDAC 阻害剤です。クラミドシンは、強力な抗増殖活性と抗癌活性を示します。クラミドシンは、カスパーゼ 3 を活性化することによってアポトーシスを誘導します。
-
GC17969
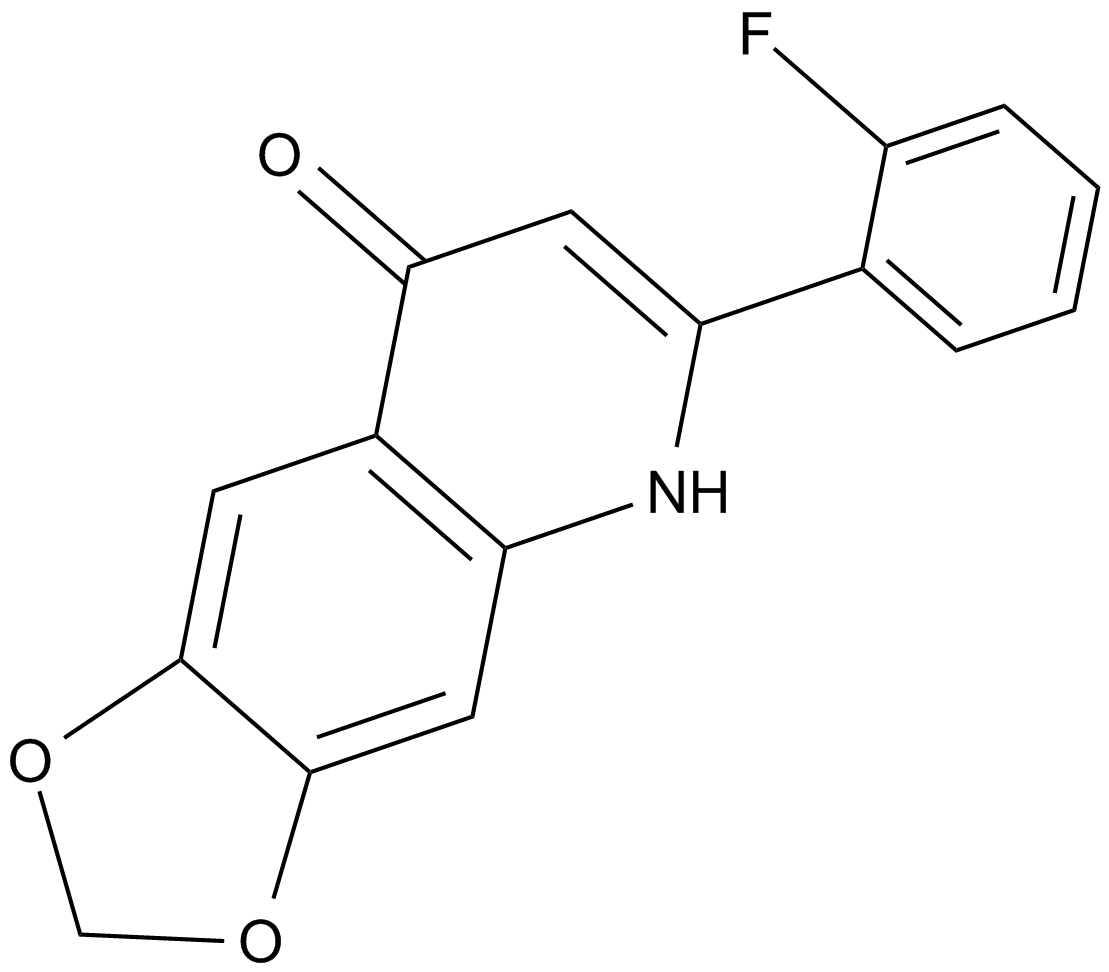
CHM 1
チューブリン重合の阻害剤
-
GC35682
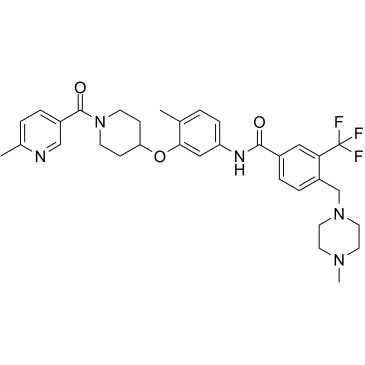
CHMFL-ABL/KIT-155
CHMFL-ABL/KIT-155 (CHMFL-ABL-KIT-155; 化合物 34) は、非常に強力な経口活性型 II ABL/c-KIT デュアル キナーゼ阻害剤 (それぞれ 46 nM および 75 nM の IC50) であり、 BLK (IC50=81 nM)、CSF1R (IC50=227 nM)、DDR1 (IC50=116 nM)、DDR2 (IC50=325 nM)、LCK (IC50=12 nM)、PDGFRβ (IC50= 80 nM) キナーゼ。 CHMFL-ABL/KIT-155 (CHMFL-ABL-KIT-155) は、細胞周期の進行を停止させ、アポトーシスを誘導します。
-
GC64028
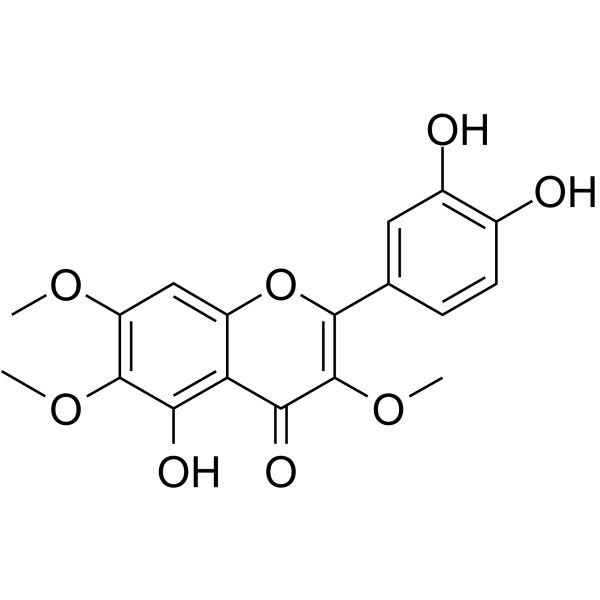
Chrysosplenol D
クリソプレノール D は、トリプル ネガティブのヒト乳癌細胞で ERK1/2 を介したアポトーシスを誘導するメトキシ フラボノイドです。
-
GC13408
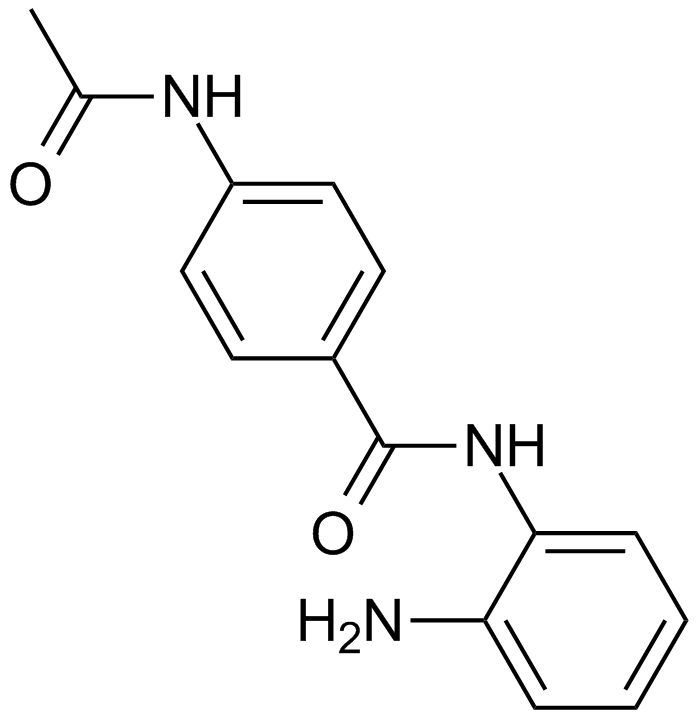
CI994 (Tacedinaline)
HDAC1、-2、および-3の阻害剤
-
GC13589
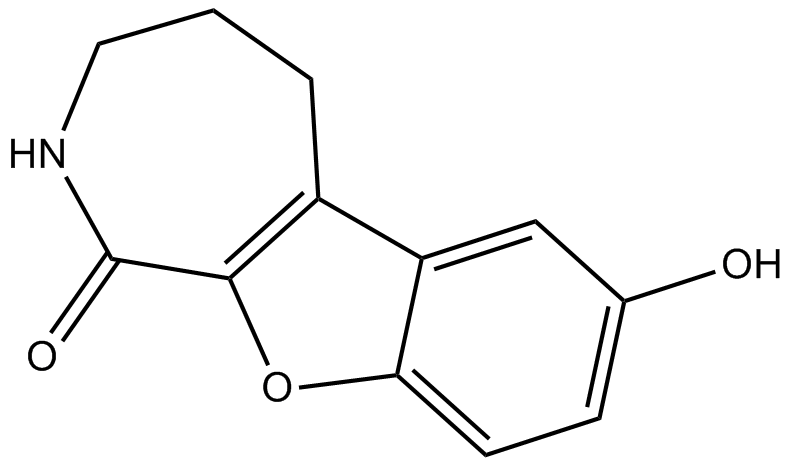
CID 755673
CID 755673 は、PKD1、PKD2、および PKD3 に対してそれぞれ 182 nM、280 nM、および 227 nM の IC50 を持つ強力な PKD 阻害剤です。
-
GC19436
CID-5721353
CID-5721353 は、147 μM の Ki に対応する 212 μM の IC50 値を持つ BCL6 の阻害剤です。
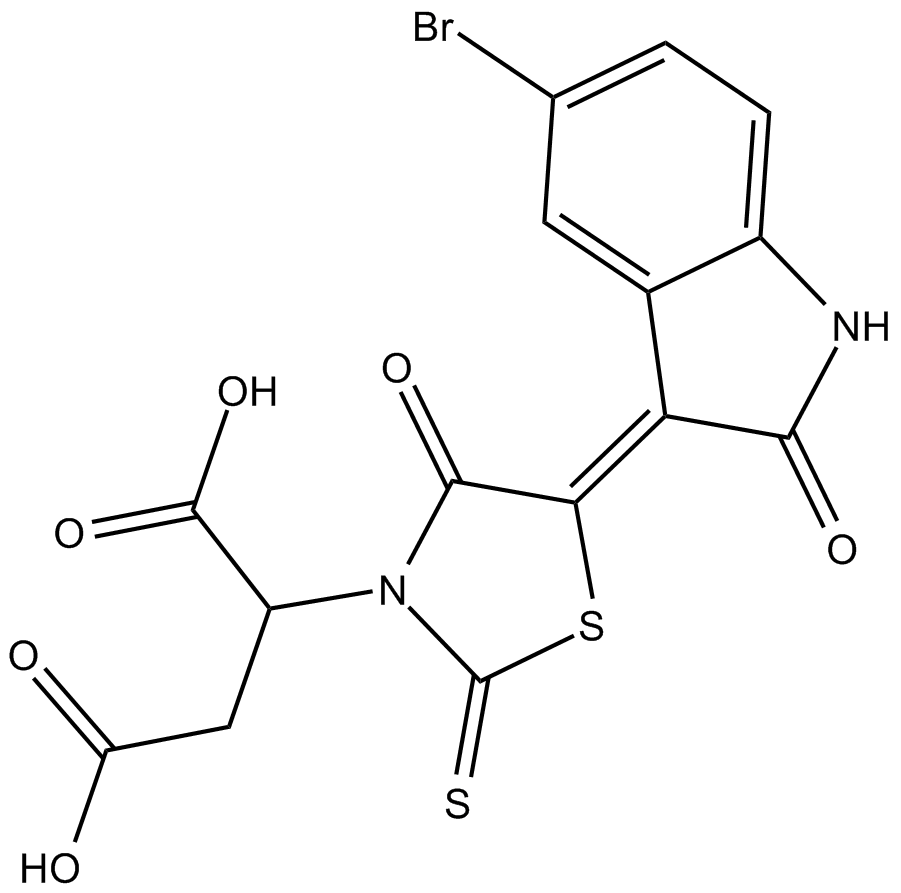
-
GC32997
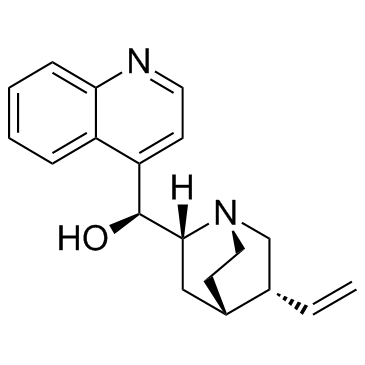
Cinchonine ((8R,9S)-Cinchonine)
シンコニン ((8R,9S)-シンコニン) は、キナの樹皮に含まれる天然化合物です。シンコニン ((8R,9S)-シンコニン) は、ヒト肝癌細胞の小胞体ストレス誘導アポトーシスを活性化します。
-
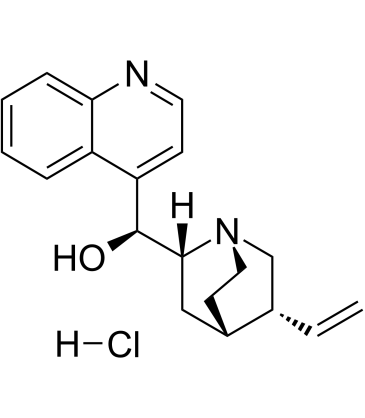
GC60708
Cinchonine hydrochloride
シンコニン塩酸塩 ((8R,9S)-シンコニン塩酸塩) は、キナの樹皮に含まれる天然のアルカロイドで、抗マラリア活性があります。シンコニン塩酸塩は、ヒト肝癌細胞の小胞体 (ER) ストレス誘発性アポトーシスを活性化します。
-
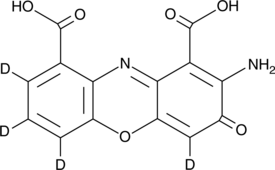
GC52269
Cinnabarinic Acid-d4
シナバリン酸の定量化のための内部標準
-
GC40986
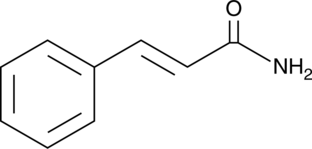
Cinnamamide
シナミルアミドはトランスシンナム酸のアミド形態であり、ストレプトマイセスの代謝物です。
-
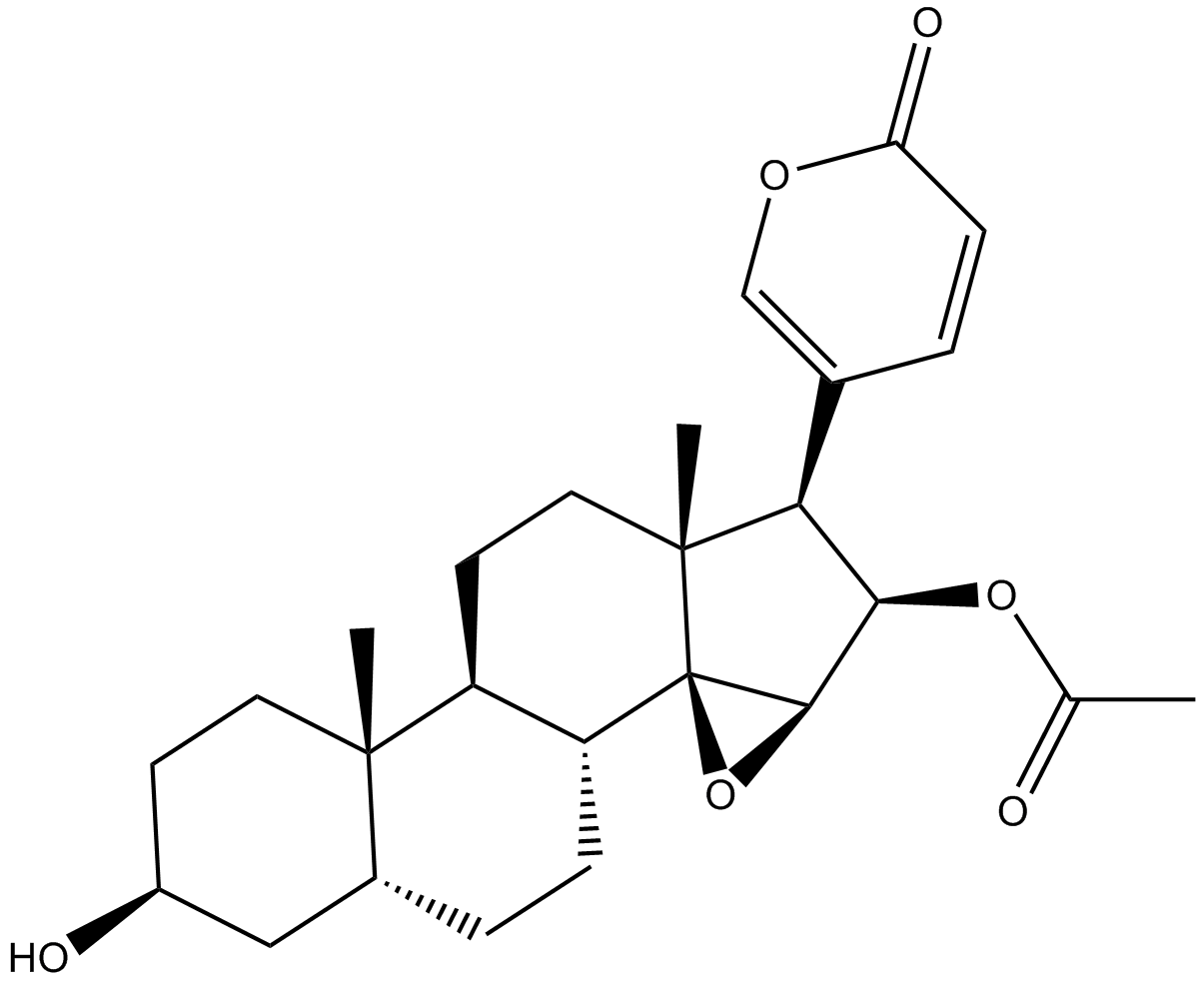
GN10189
Cinobufagin
-
GC11908
Cisplatin
Cisplatinは、最も優れた金属系抗がん剤の一つであり、精巣、卵巣、膀胱、肺、子宮頸部、頭頸部、胃、およびその他のいくつかのがんなど、広範囲の固形がんの治療に使用されている。

-
GC17491
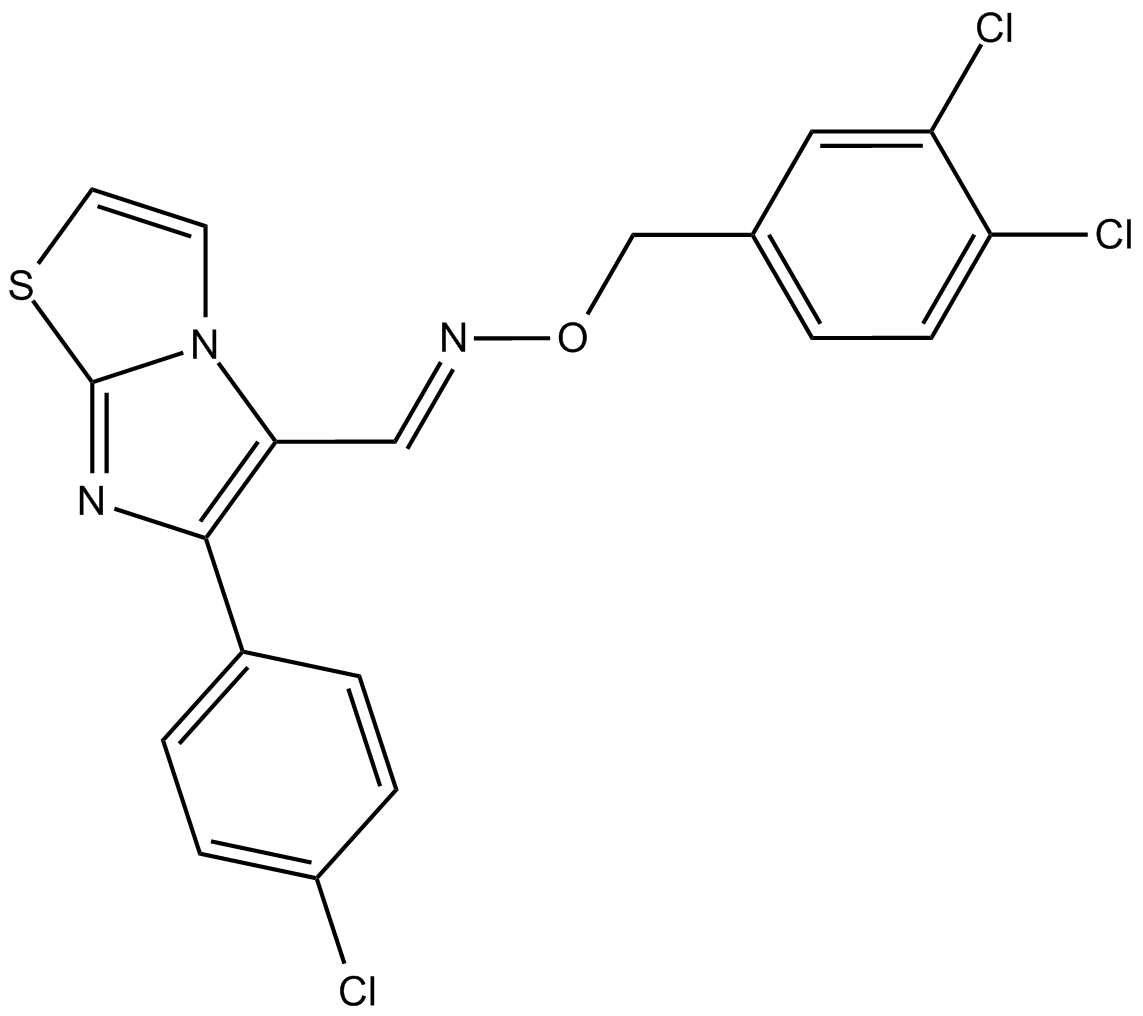
CITCO
イミダゾチアゾール誘導体である CITCO は、選択的構成アンドロスタン受容体 (CAR) アゴニストです。 CITCO は、脳腫瘍幹細胞 (BTSC) の成長と拡大を阻害し、プレグナン X 受容体 (PXR) に対して 49 nM の EC50 を持ち、他の核内受容体に対する活性はありません。
-
GC35703
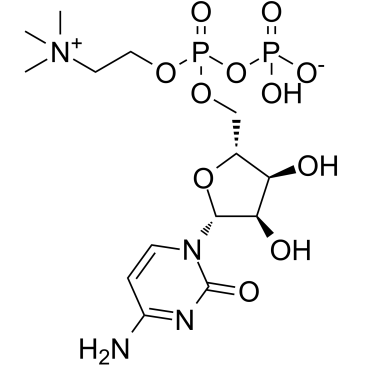
Citicoline
シチコリン (シチジン二リン酸-コリン) は、細胞膜の成分であるホスファチジルコリンの合成における中間体です。
-
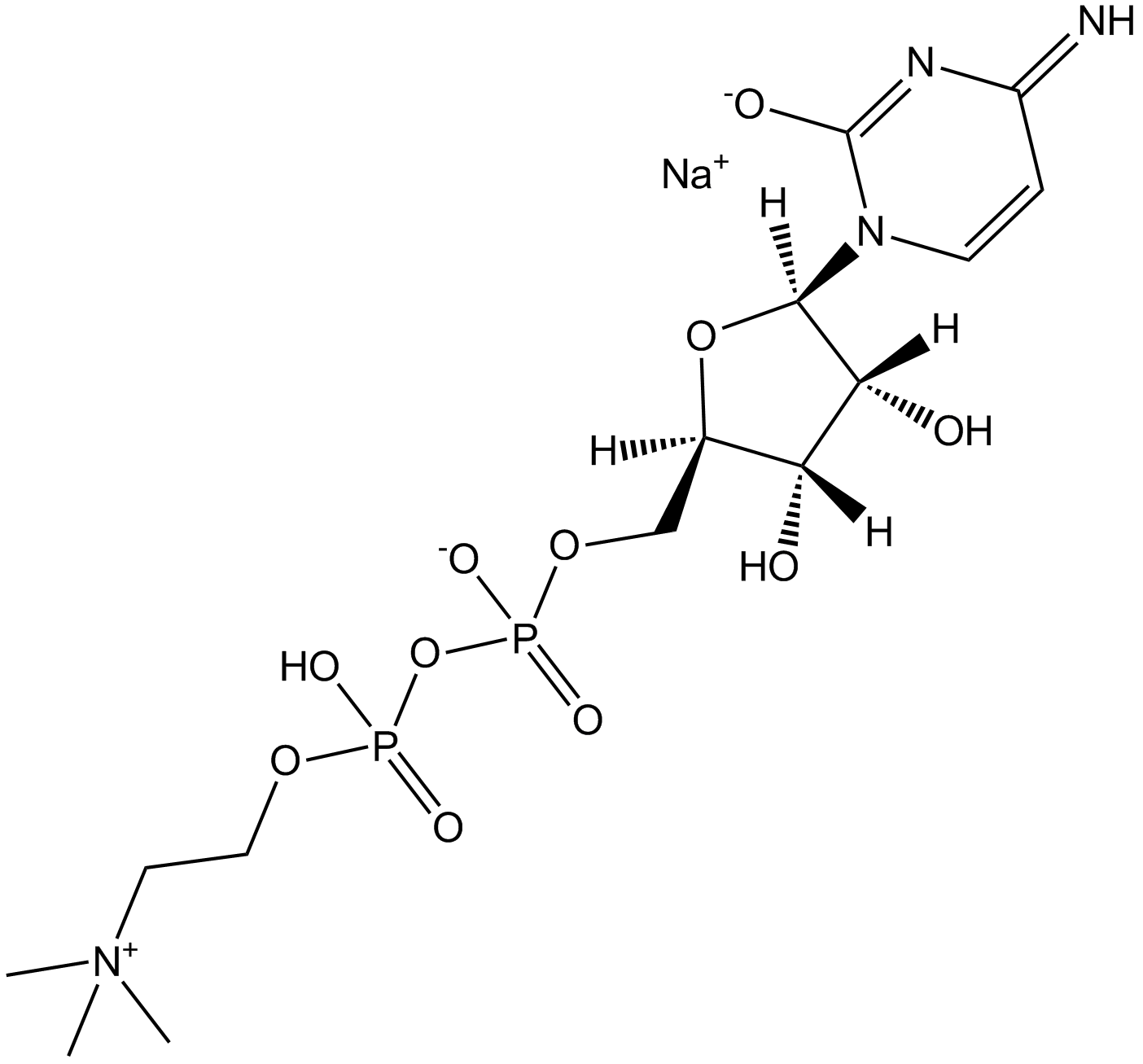
GC31186
Citicoline sodium salt
シチコリンナトリウム塩は、細胞膜の成分であるホスファチジルコリンの合成中間体であり、また神経保護効果も発揮します。
-
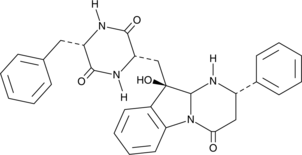
GC43273
Citreoindole
シトレオインドールは、Pの2つの株のハイブリッド細胞融合から分離されたジケトピペラジン代謝物です。
-
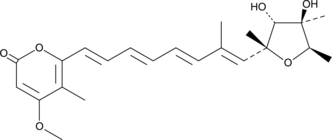
GC41514
Citreoviridin
ペニシリウム シトレオビリド NRRL 2579 由来の毒素であるシトレオビリジンは、脳シナプトソームの Na+/K+-ATPase を阻害しますが、ミクロソームでは、Na+/K+-ATPase と Mg2+-ATPase の両方の活性を阻害します。用量依存的に有意に刺激される。
-
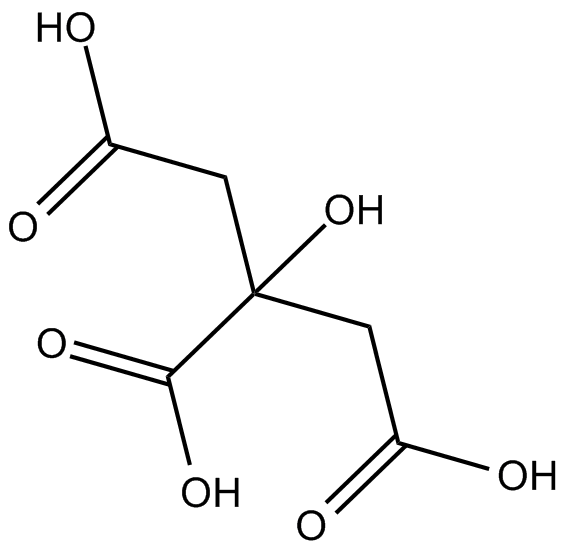
GC14203
Citric acid
クエン酸は天然の防腐剤であり、食品の酸味増強剤です。
-
GC68051
Citric acid-d4
-
GC16661
Citrinin
アポトーシスを誘発するマイコトキシン